
| A. | H2CO3?2H++CO32- | B. | Ba(OH)2?Ba2++2OH- | ||
| C. | NaHCO3?Na++HCO3- | D. | HClO?H++ClO- |
分析 先判断强弱电解质,强电解质完全电离,用等号;弱电解质部分电离,用可逆号,多元弱酸分步电离,以第一步为主,离子团不能再拆,据此进行解答.
解答 解:A.碳酸为二元弱酸,电离方程式分别书写,主要写出第一步即可,正确的淀粉方程式为:H2CO3?H++HCO3-,故A错误;
B.氢氧化钡为强电解质,电离方程式应该用等号,正确的电离方程式为:Ba(OH)2=Ba2++2OH-,故B错误;
C.碳酸氢钠为强电解质,在溶液中完全电离出钠离子和碳酸氢根离子,电离方程式应该为等号,正确的电离方程式为:NaHCO3=Na++HCO3-,故C错误;
D.次氯酸为弱酸,在溶液中部分电离出氢离子和次氯酸根离子,电离方程式为:HClO?H++ClO-,故D正确;
故选D.
点评 本题考查学生电离方程式的书写,题目难度不大,明确电解质的强弱是解题关键,注意多元弱酸分步电离,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:实验题
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V/mL | 12.9 | 15.4 | 13.1 | 13.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32gO2含2NA个原子 | |
| B. | 标准状况下,11.2LH2O含有的原子数目为1.5NA | |
| C. | 1mol的Cl-含有NA个电子 | |
| D. | 0.5mol/L的NaCl溶液中Cl-的个数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9mL | B. | 小于9mL | ||
| C. | 大于9 mL | D. | 因操作错误无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
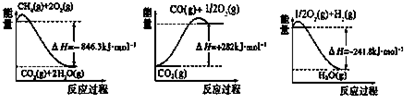
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯(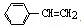 )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 标准状况下,2.24L己烷含有的分子数为0.1NA | |
| C. | 1mol甲基含10NA个电子 | |
| D. | 某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
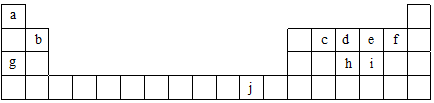
 .
. ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com