
【题目】分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“NaHCO3”的分类正确的是
A. 酸 B. 有机物 C. 盐 D. 氧化物
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 0.1 mol/L Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S)
B. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c (Na+)>c(CO32-)>c(HCO3-)>c(OH-) >c(H+)
C. 常温下,pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>②>③
D. 将CH3COONa溶液从20℃升温至30℃,溶液中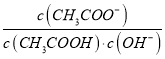 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下浓度为0.1mol·L-1的下列溶液的pH如下表:
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
下列有关说法正确的是
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B. 若将CO2通入0.1 mol·L-1Na2CO3溶液中至溶液中性,则溶液中2c(CO32-)+c(HCO3-)=0.1 mol·L-1
C. 根据上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常数K=10-7.6
HClO+OH-的水解常数K=10-7.6
D. 向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>c(H+)>c(HClO)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量在化学中占有重要地位.根据计算填空:
(1)1.204×1022个NH3分子的物质的量为 , 在标准状况下的体积为mL.
(2)含0.4mol Fe3+的Fe2(S04)3中含SO42﹣的物质的量为 .
(3)已知8gX与10gY恰好完全反应生成0.02mol Z和15.88g W,则Z的摩尔质量为 .
(4)某混合溶液中只含有下列几种离子(不考虑水的电离):Na+、Mg2+、Cl﹣、SO42﹣ , 若Na+、Mg2+、Cl﹣的物质的量浓度依次为0.2mol/L、0.25mol/L、0.5mol/L,则(SO42﹣)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的丁作原理如图所示.下列说法正确的是( ) 
A.电子从b极经导线流向a极
B.正极的电极反应式为O2+4e﹣+2H2O═4OH﹣
C.还可以选用NaOH固体作固态电解质
D.若反应中转移1 mol电子,则生成22.4L(标准状况)CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com