
【题目】25℃时。有c(CH3COOH)+ c(CH3COO-)=0.1mol/L的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-) 与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述中正确的是。

A. pH=5.5的溶液中c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点所表示的溶液中c(Na+) + c(H+)=c(CH3COO-)+c(OH-)
C. pH=3.5的溶液中: c(Na+) + c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L
D.向W点所表示的1L溶液中通入0.05molHCl气体(溶液的体积变化可忽略):c(H+)=c(OH-)+c(CH3COOH)
【答案】B C
【解析】
试题分析:A、pH=5.5比4.75大,W点时c(CH3COOH)=c(CH3COO-),从曲线来看当pH=5.5时,c(CH3COOH)<c(CH3COO-),故A错误;故A正确;B、W点由电荷守恒可知,c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故B正确;C、由电荷守恒及c(CH3COOH)+c(CH3COO-)=0.1molL-1可知,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=c(CH3COO-)+c(OH-)-c(OH-)+c(CH3COOH)=0.1mol/L,故C正确;D、W点为等量的醋酸和醋酸钠的混合液,1.0 L 溶液中通入0.05 mol HCl 气体得到0.05molNaCl和0.1molHAc,由电荷守恒可知,c(H+)=c(CH3COO-)+c(OH-),故D错误;


科目:高中化学 来源: 题型:
【题目】某有机物的质量为3.0g,完全燃烧后产物通过浓硫酸,浓硫酸质量增加3.6g;其余的气体再通过碱石灰,被完全吸收,碱石灰质量增加6.6g。已知该有机物的蒸气对氢气的相对密度是30。
(1)求该有机物的分子式。(要求写计算过程)
(2)若该有机物能与金属钠反应,经催化氧化后的生成物含有醛基,请写出该有机物的结构简式,并对它进行命名。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含x mol NH4Fe(SO4)2的溶液中逐滴加入y mol Ba(OH)2溶液,下列说法正确的是( )
A. 当x=2y时,发生的离子反应为2NH![]() +SO
+SO![]() +Ba2++2OH-===2NH3·H2O+BaSO4↓
+Ba2++2OH-===2NH3·H2O+BaSO4↓
B. 当x≥y时,发生的离子反应为2Fe3++3SO![]() +3 Ba2++6OH-===2Fe(OH)3↓+3BaSO4↓
+3 Ba2++6OH-===2Fe(OH)3↓+3BaSO4↓
C. 当2x=y时,发生的离子反应为2Fe3++2NH![]() +2SO
+2SO![]() +2Ba2++6OH-===2Fe(OH)3↓+2BaSO4↓+2NH3·H2O
+2Ba2++6OH-===2Fe(OH)3↓+2BaSO4↓+2NH3·H2O
D. 当x<y<1.5x时,沉淀质量为(233x+107×![]() ) g
) g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 常温下,0.1 mol/L Na2S溶液中存在:c(OH-) = c(H+) + c(HS-) + c(H2S)
B. 常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在: c (Na+) = c(A-) > c(OH-) = c(H+)
C. 常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol/L:c(Na+) = c(CH3COOH) > c(CH3COO-) > c(H+) = c(OH-)
D. 常温下,将0.1 mol/L CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中![]() 的值减小到原来的
的值减小到原来的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 人类目前所直接利用的能量全部是由化学反应产生的
B. 化学反应不一定伴随着能量变化
C. 化学变化中的能量变化主要是由化学键变化引起的
D. 化学反应中能量变化的大小与反应物质量的多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. ![]() C表示质子数为6、中子数为8的核素
C表示质子数为6、中子数为8的核素
B. 甲醇(CH3OH)和甘油(CH2OHCHOHCH2OH)互为同系物
C. C5H12的同分异构体有3种,其沸点各不相同
D. CH3CH2CH2CH(CH3)2的名称是2甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学探究小组同学为探究乙酸乙酯的制备与水解情况,甲、乙同学分别使用图1、图2装置制备乙酸乙酯。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH。②相关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 117.9 | 77 |
(1)甲同学在制得乙酸乙酯后,分离乙酸乙酯与饱和碳酸钠溶液的操作是_______________。
(2)试管中装有饱和Na2CO3溶液,其作用是________(填序号)。
A.吸收乙醇 B.除去乙酸
C.乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)甲同学分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出______________;再加入____________(填序号);然后进行蒸馏,收集77 ℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(4)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,乙同学利用图2所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡试管B,再测有机层的厚度,实验记录如下:

①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol·L-1。
②分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)为原料(已知两种原料中均不含有单质杂质)制备高纯度硫酸锰的工艺流程如图所示。
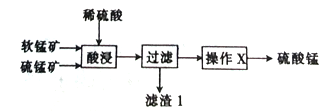
(1)已知滤渣1中含有一种非金属单质,该非金属单质的化学式为_____________________。
(2)已知二氧化锰与硫化锰的物质的量之比对酸浸时的浸出率有影响,相关实验数据如下表所示。当二氧化锰与硫化锰的物质的量之比为______________时,为最优反应配比。
号 | 二氧化锰与硫化锰的物质的量之比 | 浸出液的pH | 浸出率% |
1 | 1.25:1 | 2.5 | 95.30 |
2 | 1.75:1 | 2.5 | 97.11 |
3 | 2.25:1 | 2.5 | 99.00 |
4 | 2.5:1 | 2.5 | 98.40 |
(3)操作X为蒸发浓缩、______________、过滤,洗涤、烘干,在洗涤操作中,常用酒精洗涤MnSO4·H2O晶体,其主要目的是_________。
(4)现有10t锰矿,其中MnO2和MnS的含量均为29%,若流程中Mn的损耗率为10%,则最终制得硫酸锰(MnSO4·H2O)_________t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应方程式中,不正确的是( )
A. 丙烯与Br2加成:CH2===CHCH3+Br2―→CH2BrCH2CH2Br
B. 甲烷与Cl2发生取代反应:CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
C. 催化裂化:C16H34 ![]() C8H16+C8H18
C8H16+C8H18
D. 淀粉水解:(C6H10O5)n+nH2O![]() nC6H12O6
nC6H12O6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com