
���϶��¡���һ����������������й����¡�2007��10��24���ҹ����϶�һ�š�̽�������ɳ����������Ԥ���Ĺ������������������ƽ������õ���Һ��/Һ�⡣��֪��298Kʱ��2g������������ȫ��Ӧ����Һ̬ˮ����285.8kJ����˷�Ӧ���Ȼ�ѧ����ʽΪ
A��2H2(g)+O2(g) === 2H2O(l) ��H=��285.8KJ��mol��1
B��2H2(g)+O2(g) === 2H2O(l) ��H=+285.8KJ��mol��1
C��H2(g)+ O2(g) === H2O(l) ��H=��285.8KJ��mol��1
O2(g) === H2O(l) ��H=��285.8KJ��mol��1
D��H2(g)+  O2(g) === H2O(g) ��H=��285.8KJ��mol��1
O2(g) === H2O(g) ��H=��285.8KJ��mol��1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��X��Y��Z��M ��N��ԭ���������ε��������ֶ�����Ԫ�أ�����Z��M��Nͬ���ڣ�X�� Zͬ������X��ԭ�Ӱ뾶��С��ԭ�ӣ�Y��Nͬ���壬Z����Y2��������ͬ�ĵ��Ӳ�ṹ��M�ĵ��ʾ����۵�ߡ�Ӳ�ȴ���һ����Ҫ�İ뵼����ϡ�
��1��M��Ԫ�����ơ���������N��Ԫ�����ڱ��е�λ�á�������������������
��2�����Ӱ뾶�Ƚϣ�r��Z������������r��Y2���������>������=����<����
��3��X��Z�γɵĻ�����A�ǡ����� �� ������������ӻ�������ۻ��������A��X2Y��Ӧ�Ļ�ѧ����ʽ�ǡ����������� ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�Ȼ�ѧ����ʽ��
H2O(g)��H2(g) + 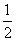 O2(g) ��H = +241.8kJ/mol
O2(g) ��H = +241.8kJ/mol
H2(g)+ 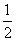 O2(g) �� H2O(1) ��H = ��285.8kJ/mol
O2(g) �� H2O(1) ��H = ��285.8kJ/mol
��1gҺ̬ˮ��Ϊˮ����ʱ���������仯��( )
A������88kJ B�� ����2.44kJ
C������44kJ D�� ����44kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
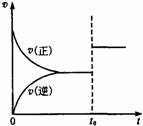
���淴ӦaX(g)��bY(g)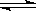 cZ(g)����һ���¶��µ��ܱ������ڴﵽƽ���t0ʱ�ı�ijһ�����������ѧ��Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ����ͼ��ʾ������˵������ȷ����( )
cZ(g)����һ���¶��µ��ܱ������ڴﵽƽ���t0ʱ�ı�ijһ�����������ѧ��Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ����ͼ��ʾ������˵������ȷ����( )
A����a��b��c����t0ʱֻ�����˷�Ӧ���Ũ��
B����a��b��c����t0ʱֻ�������¶�
C����a��b��c����t0ʱֻ������������ѹǿ
D����a��b��c����t0ʱֻ�����˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10L�����У�����2mol��SO2(g)��2mol��NO2(g)�������¶Ⱥ㶨��������Ӧ��
SO2(g)+ NO2(g) 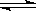 SO3(g)+NO(g)�����ﵽƽ��״̬ʱ�����������SO2(g)��ת����Ϊ50%��
SO3(g)+NO(g)�����ﵽƽ��״̬ʱ�����������SO2(g)��ת����Ϊ50%��
�����¶��¡��������У��ټ�������1mol��SO2(g)����
��1����ѧƽ�⽫��________�����ƶ���NO2��ת���ʽ�____________��
��2�������㣬���ﵽ�µ�ƽ��״̬ʱ��������SO2(g)��Ũ����_______mol/L��
��3�����������У�SO2��ת������50%��Ϊ_______%��NO2��ת������__________%��Ϊ_______%��
��4�������������ǵ���ʾ�ǣ�����һ�ַ�Ӧ�������������ת���ʽ�________________������� �������䡱��С������һ��Ӧ���ת���ʽ�____________������� �������䡱��С��������ʵ�����е������ǣ�����ͨ������________������������߳ɱ��ߵķ�Ӧ��������ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڲ�ͬ����²��A(g)+3B(g) 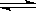 2C(g)+2D(g)�����з�Ӧ���ʣ����з�Ӧ����������
2C(g)+2D(g)�����з�Ӧ���ʣ����з�Ӧ����������
A����(D)=0.4 mol��L��1��s��1 B����(C)=0.5 mol��L��1��s��1
C����(B)=0.6 mol��L��1��s��1 D����(A)=0.15 mol��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������������彡����ɽϴ�Σ������ �� ��
A����С�մ�NaHCO3����������������ͷ
B����ʳ����ϴ��ˮƿ���ڱڸ��ŵ�ˮ����CaCO3��
C����SO2Ư�������������ʳƷ
D������ˮ��ͨ������Cl2����ɱ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����
A��������̼������Һ��Ӧ��2H+��CO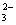 == CO2����H2O
== CO2����H2O
 B��������Һ������������ͭ��Ӧ��2CH3COOH��Cu(OH)2 Cu2+��2CH3COO����2H2O
B��������Һ������������ͭ��Ӧ��2CH3COOH��Cu(OH)2 Cu2+��2CH3COO����2H2O
C����������Һ��ͨ������������̼��2C6H5O����CO2��H2O 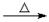 2C6H5OH��CO32��
2C6H5OH��CO32��
D����ȩ��Һ��������������Һ���ȣ�
HCHO+4++4OH-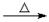 CO
CO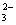 +2NH
+2NH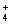 +4Ag��+6NH3+2H2O
+4Ag��+6NH3+2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com