


科目:高中化学 来源:2013届江西省高二下学期期中考试化学试卷(解析版) 题型:选择题
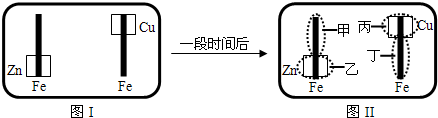
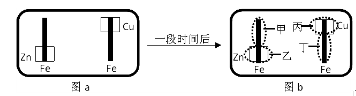
某校活动小组为探究金属腐蚀的相关原理,设计了如下图a所示装置,图a的铁棒末段分别连上一块Zn片和Cu片,并静置于含有K3Fe(CN)6及酚酞的混合凝胶上。一段时间后发现凝胶的某些区域(如下图b示)发生了变化,已知Fe2+可用K3Fe(CN)6来检验(呈蓝色)。则下列说法不正确的是( )
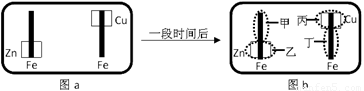

A.甲区发生的电极反应式:Fe-2e-= Fe2+ B.乙区产生Zn2+
C.丙区呈现红色 D.丁区呈现蓝色
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
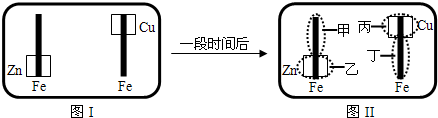
| A.甲区不变色 | B.乙区呈现蓝色 |
| C.丙区产生Cu2+离子 | D.丁区产生Fe2+离子 |
查看答案和解析>>
科目:高中化学 来源:2011年北京市高考化学模拟试卷(一)(解析版) 题型:选择题
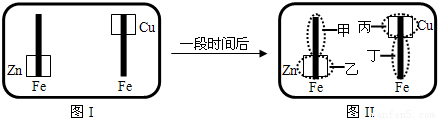
查看答案和解析>>
科目:高中化学 来源:江西省期中题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com