
【题目】向一定质量、一定溶质质量分数的稀盐酸中逐滴加入某碳酸钠溶液。实验过程中,产生气体质量与加入碳酸溶液的质量关系如下图所示,试计算:
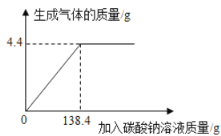
(1)恰好完全反应时,所加碳酸钠溶液中Na2CO3质量是多少?
(2)若恰好完全时所得溶液的溶质质量分数为5%,则稀盐酸的溶质质量分数是多少?
【答案】(1)10.6g;(2) 7.3%。
【解析】
试题分析:(1)根据图示可知产生气体最大值4.4g时盐酸溶液的溶质与138.4g Na2CO3恰好完全反应时。根据方程式:Na2CO3+ 2HCl=2NaCl+H2O+ CO2↑可知:106g碳酸钠与73gHCl恰好反应产生44gCO2,则反应产生4.4gCO2水,反应消耗的碳酸钠质量是10.6g;(2)根据方程式:Na2CO3+ 2HCl=2NaCl+H2O+ CO2↑可知,恰好完全反应时,反应产生的NaCl的质量是(117÷44)×4.4g=11.7g,所得溶液的质量=11.7g÷5%=234g,稀盐酸的溶夜质量=234g+4.4g-138.4g=100g则稀盐酸的溶质质量分数是(7.3g÷100g)×100%=7.3%。


科目:高中化学 来源: 题型:
【题目】化学式与俗名相符的是
A. 小苏打Na2CO3,苛性钠NaOH
B. 芒硝Na2SO4·10H2O,消石灰Ca(OH)2
C. 苏打NaHCO3,石灰石CaCO3
D. 纯碱NaOH,食盐NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取钠-镁合金7.0克进行如下实验:

(1)写出Mg在CO2中燃烧的化学方程式
(2)向溶液1中加过量的NaOH溶液,发生反应的离子方程式为
(3)写出合金的化学组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的恒容容器中,充入1molA和3molB,并在一定条件下发生如下反应:
A(s)+3B(g)![]() 2C(g)
2C(g)
若经3s后测得C的浓度为0.6molL-1,下列选项说法正确的组合是
①用A表示的反应速率为0.1molL-1s-1
②用B表示的反应速率为0.4molL-1s-1
③3s时生成C的物质的量为1.2 mol
④3s时B的浓度为0.6molL-1
A.①②④ B.①③④ C.③④ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.MgF2晶体中的化学键是共价键
B.某物质在熔融态能导电,则该物质中一定含有离子键
C.干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力
D.N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c三种物质的溶解度曲线如下图所示。取等质量t2℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t2℃。下列说法不正确的是( )

A.原饱和溶液中,溶质的质量分数a>b=c
B.恢复至t2℃时,析出溶质的质量a > b=c
C.恢复至t2℃时,三种溶液一定都是饱和溶液
D.若继续降温至t1℃,三种溶液一定都是饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构现象广泛存在于有机化合物中。下列有关同分异构体的说法正确的是
A.具有相同结构式
B.具有相同分子式
C.具有不同相对分子质量
D.具有不同原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中,从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,能加快溶出率的操作有 、 。(写出两条)
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴,则浸出钴的离子反应方程式为 (产物中只有一种酸根)。请从反应原理分析不用盐酸浸出钴的主要原因 。
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在空气中久置变质,在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是( )
A. 食盐 B. 漂白粉 C. 氯水 D. 生石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com