
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑤不能发生 | D. | 只有⑥不能发生 |
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1mol氯气发生化学反应,转移的电子数必为2NA | |
| D. | CH4的摩尔质量与NA个CH4分子的质量在数值上相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2O | B. | NaOH | C. | K2CO3 | D. | CH3COONa |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I->Fe2+>Cl->SO2 | B. | Cl->Fe2+>SO2>I- | C. | Fe2+>I->Cl->SO2 | D. | SO2>I->Fe2+>Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子氧化性:A(n+1)+>Bn+离子还原性:C(n+1)->Dn- | |
| D. | C最高价氧化物的水化物的酸性比D的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 强电解质 | 弱电解质 | 非电解质 |
| A | CaCO3 | H2SiO3 | 酒精 |
| B | NaCl | NH3 | BaSO4 |
| C | Fe | CH3COOH | 蔗糖 |
| D | HNO3 | Fe(OH)3 | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
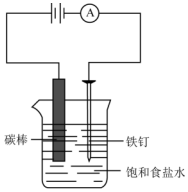 如图所示,回答下列问题:
如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com