


科目:高中化学 来源: 题型:
 青花瓷,俗称青花,是中国瓷器的主流品种之一,某同学利用如下方法来粗略测定如图所示的青花瓷瓶的容积.把11.7gNaCl晶体放入到500mL烧杯中,加入500mL蒸镏水,待NaCl完全溶解后,将溶液全部转移到该瓶中,用蒸馏水稀释至完全充满容器(假定溶液浓度均一).从中取出100mL溶液,该溶液恰好能与10mL0.100ml/L的AgNO3溶液完全反应,则下列说法正确的是( )
青花瓷,俗称青花,是中国瓷器的主流品种之一,某同学利用如下方法来粗略测定如图所示的青花瓷瓶的容积.把11.7gNaCl晶体放入到500mL烧杯中,加入500mL蒸镏水,待NaCl完全溶解后,将溶液全部转移到该瓶中,用蒸馏水稀释至完全充满容器(假定溶液浓度均一).从中取出100mL溶液,该溶液恰好能与10mL0.100ml/L的AgNO3溶液完全反应,则下列说法正确的是( )| A、该青花瓷瓶的容积约 20 L |
| B、常温下,该青花瓷瓶几乎能容纳2kg H2O |
| C、常温常压下,该青花瓷瓶几乎能容纳56g N2 |
| D、青花为高级瓷器,该青花瓷瓶可以盛装氢氟酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、c=
| ||
B、m=V?ρ
| ||
C、w%=
| ||
D、c=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测量盐酸的温度后,温度计没有用水冲洗干净 |
| B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 |
| C、量取盐酸时仰视读数 |
| D、将50 mL 0.55 mol/L氢氧化钠溶液取成了50 mL0.55 mol/L的氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4?FeSO4?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | - | - |
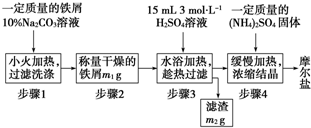
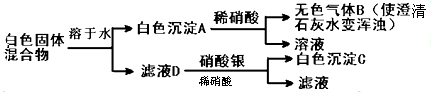
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO
| ||
B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
| ||
C、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,不一定有NH
| ||
| D、向待测液中加入KSCN溶液无现象,加入氯水后变为血红色,则待测液中含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com