
 乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子结构中各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,②键和⑤断裂 |
| C、在铜催化下和氧气反应时,键①和③断裂 |
| D、与氢卤酸反应时,①键断裂 |


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Na2O2跟 H2O反应转移电子的数目为2NA |
| B、1 mol氯气跟NaOH反应转移电子的数目为NA |
| C、常温常压下,22.4 L氯气所含原子数为2NA |
| D、标准状况下,22.4 L蒸馏水所含分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B、生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应 |
| C、反应产物的总能量大于反应物的总能量时,△H>0 |
| D、△H的大小与热化学方程式的计量系数无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该晶体类型是原子晶体 |
| B、该晶体中碳原子和氧原子的个数比为1:2 |
| C、每摩尔该晶体中含4molC-O |
| D、晶体的空间最小环共有6个原子构成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+2 | B、+3 | C、+4 | D、+5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.00molNaCl中含有6.02×1023个NaCl分子 |
| B、欲配置1.00L1.00mol/L的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
| C、1molNO2和N2O4混合气体中含有原子总数为3NA |
| D、1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,共转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加压有利于SO2与O2反应生成SO3 |
| B、用过量空气煅烧硫铁矿可以提高原料的利用率 |
| C、加入催化剂都能使合成氨的反应速率加快 |
| D、温度过高对合成氨反应不利 |
查看答案和解析>>
科目:高中化学 来源: 题型:
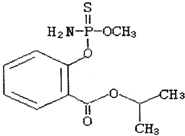 毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )
毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )| A、该化合物属于芳香烃 |
| B、该化合物中至少有7个碳原子在同一平面 |
| C、该化合物的分子式为C11H14O4NPS |
| D、该化合物能发生加聚反应、水解反应和酯化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com