
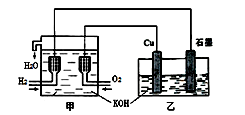
| A.乙中Cu电极的电极反应式是: 2Cu + 2OH-→ Cu2O+ H2O+ 2e- |
| B.甲中通入氢气的电极为正极 |
| C.乙中阴离子向石墨电极移动 |
| D.电路上通过0.5 mol电子,可制得0.5 mol Cu2O |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
 水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成: ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钢铁与电源的正极连接,钢铁可被保护 |
| B.钢铁发生析氢腐蚀时,负极反应为:Fe-3e-=Fe3+ |
| C.与铜质水龙头连接的钢质水管不易发生腐蚀 |
| D.钢铁在潮湿的空气中能发生电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
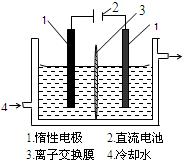
| 实验方法 | 实验现象及结论 |
| | |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
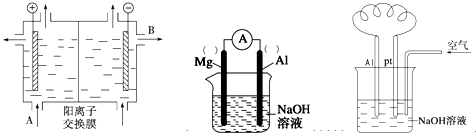
 B____________________
B____________________ ____________________。
____________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

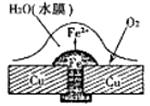
| A.铜丝上发生的反应为:O2+4e+2H2O→4OH- |
| B.铁钉上发生的反应为:Fe-3e→Fe3+ |
| C.NaCl的存在能加快铁钉的腐蚀速率 |
D.一段时间后铁钉上出现 红棕色物质 红棕色物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com