
| A. | 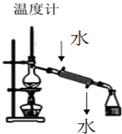 装置用于分离两种沸点相差较大的液体互溶混合物 | |
| B. | 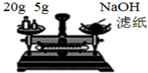 装置称量氢氧化钠固体 | |
| C. | 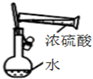 装置配制一定物质的量浓度的稀硫酸 | |
| D. |  装置检查容量瓶是否漏水 |
分析 A.冷凝水应下进上出;
B.NaOH应放在小烧杯中称量;
C.浓硫酸溶于水放热;
D.在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水.
解答 解:A.蒸馏时需在蒸馏烧瓶中加热,用冷凝管冷却,冷凝管冷凝水的流向是下进上出,故A错误;
B.NaOH具有腐蚀性和吸水性,能与空气中二氧化碳反应,称量时应尽量减小与空气的接触面积,应放在小烧杯中称量,故B错误;
C.浓硫酸溶于水放热,应在小烧杯中稀释并冷却,故C错误;
D.在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验,故D正确.
故选D.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 100mL溶液中一定只有0.02molK+ | B. | 溶液中CO${\;}_{3}^{2-}$浓度为0.1mol/L | ||
| C. | 不能确定Cl-是否存在 | D. | Ba2+和Mg2+一定不存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在0.24L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题.
在0.24L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2为直线形分子,SO2也为直线形分子 | |
| B. | 固态CS2是分子晶体,固态SiO2也是分子晶体 | |
| C. | NCl3中N原子是sp3杂化,BCl3中B原子也是sp3杂化 | |
| D. | Al(OH)3能溶于NaOH溶液,Be(OH)2也能溶于NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素、油脂、蛋白质均为高分子化合物 | |
| B. | 35%~40%的甲醛水溶液称为福尔马林,具有杀菌、防腐性能 | |
| C. | 淀粉、溴乙烷、脂肪在一定条件下都可以发生水解反应 | |
| D. | 脂肪烃的来源有石油、天然气和煤等,通过石油的裂化及裂解可得到气态烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 强电解质 | 磷酸 | H2SO4 | Ba(OH)2 | 食盐水 |
| 弱电解质 | Cu(OH)2 | NH3•H2O | CaCO3 | 干冰 |
| 非电解质 | Cu | SO2 | 蔗糖 | 苯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲和丙的K相同 | B. | 乙和丙的正反应速率相同 | ||
| C. | 乙中SO3的体积分数小于丙 | D. | 转化率:α甲(SO2)+α乙(SO3)<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮、碳都是重要的非金属元素,含氮、碳元素的物质在工业生产中有重要的应用.
氮、碳都是重要的非金属元素,含氮、碳元素的物质在工业生产中有重要的应用.| 容器 | 起始投入 | 达平衡时 | |||
| 甲 | 2mol N2 | 3mol H2 | 0mol NH3 | 1.5mol NH3 | 同种物质的体积分数相同 |
| 乙 | a mol N2 | b mol H2 | 0mol NH3 | 1.2mol NH3 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com