
 两种有机物,二者分别属于哪一类.你得到什么结论?
两种有机物,二者分别属于哪一类.你得到什么结论? 科目:高中化学 来源: 题型:解答题
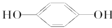 E; ③
E; ③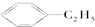 H;
H;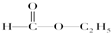 I;⑤
I;⑤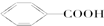 G; ⑥
G; ⑥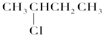 J.
J.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
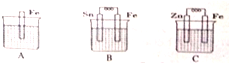
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 物质的量是度量物质所含微观粒子多少的物理量 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | 等质量的O2和O3中所含氧原子个数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 观察比较外观形态 | B. | 用手触摸比较 | ||
| C. | 放到嘴里品尝一下 | D. | 用化学方法进行鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  |  |  | |
| 化工 | 氯碱工业 | 高炉炼铁 | 铜的精炼 | 生产漂白粉 |
| 原理 | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2NaOH+Cl2↑+ H2↑ | 3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 阴极: Cu2++2e-═Cu | 2NaOH+Cl2═NaCl+NaClO+H2O |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验 | 1 | 2 | 3 | 4 |
| V(KMnO4)/mL | 19.50 | 21.50 | 19.48 | 19.52 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应不一定有分子碰撞 | B. | 化学反应的活化能一定大于零 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 发生有效碰撞的分子是活化分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com