
c(CuSO4)=0.1 mol·L-1;c(Na2SO4)=0.05 mol·L-1。
解析:CuSO4溶液的物质的量浓度是:
![]()
取100 mL 0.1 mol·L-1CuSO4溶液,其中含CuSO4的物质的量:
n(CuSO4)=0.1 mol·L-1×![]() =0.01 mol
=0.01 mol
100 mL 0.2 mol·L-1NaOH溶液中含NaOH的物质的量:
n(NaOH)=0.2 mol·L-1×![]() =0.02 mol
=0.02 mol
CuSO4 + 2NaOH====Na2SO4 +Cu(OH)2↓
1 mol 2 mol 1 mol
0.01 mol 0.02 mol
由方程可知CuSO4与NaOH 恰好反应,生成0.01 mol Na2SO4。
Na2SO4溶液的物质的量浓度:
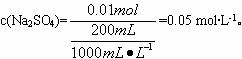


科目:高中化学 来源:志鸿系列全优设计必修一化学人教版 人教版 题型:021
|
25℃时,将a g硫酸铜晶体(CuSO4·5H2O)溶于b g水中,恰好形成V mL饱和溶液.下列关系正确的是 | |
A. |
该饱和溶液中硫酸铜物质的量浓度为c= |
B. |
该饱和溶液中硫酸铜的质量分数为w= |
C. |
25℃硫酸铜的溶解度为S= |
D. |
该饱和硫酸铜溶液的密度为ρ= |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.该饱和溶液中硫酸铜物质的量浓度为c=![]() mol·L-1?
mol·L-1?
B.该饱和溶液中硫酸铜的质量分数为w=![]()
C![]() g?
g?
D.该饱和硫酸铜溶液的密度为ρ=![]() g·L-1
g·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
A.该饱和溶液硫酸铜物质的量浓度为 c=![]()
B.该饱和溶液中硫酸铜的质量分数为 ![]()
C.25℃硫酸铜的溶解度为 S=![]()
D.该饱和硫酸铜溶液的密度为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
将25 g硫酸铜晶体溶解于水中,配成1 L溶液,此溶液的物质的量浓度是多少?取其溶液100 mL,向其中加入100 mL 0.2 mol·L-1的NaOH溶液,反应后溶液的物质的量浓度又是多少?(设混合后溶液体积不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com