
| 净含量:500mL | |
| 饮用水矿物质成分(mg.L-1) | |
| 钙Ca | ≥4.0 |
| 镁Mg | ≥1.0 |
| 钠Na | ≥3.0 |
| m |
| M |
| 2×10-3g |
| 40g/mol |
| 1 |
| 2 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(1)矿泉水中往往含多种有益于人体健康的成分。右图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥ ▲ mol。

(2)现代生活离不开铝,工业上以铝土矿为原料生产铝。
现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500 mL溶液。取
100 mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子)。
已知部分离子的物质的量浓度为:
c(H+) = 0.02 mol·L-1 c(Mg2+) = 0.01 mol·L-1
c(Fe3+)= 0.02 mol·L-1 c(Cl-) = 0.52 mol·L-1
①溶液中Al3+物质的量浓度为 ▲ mol·L-1k*s5*u
②则该铝土矿样品中Al2O3的质量为 ▲ g(精确至0.01 g)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)矿泉水中往往含多种有益于人体健康的成分。右图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥ ▲ mol。
(2)现代生活离不开铝,工业上以铝土矿为原料生产铝。
现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500 mL溶液。取
100 mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子)。
已知部分离子的物质的量浓度为:
c(H+) = 0.02 mol·L-1 c(Mg2+) = 0.01 mol·L-1
c(Fe3+)= 0.02 mol·L-1 c(Cl-) = 0.52mol·L-1
①溶液中Al3+物质的量浓度为 ▲ mol·L-1k*s5*u
②则该铝土矿样品中Al2O3的质量为 ▲ g(精确至0.01 g)。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省宁波市高一上学期期末考试化学试卷 题型:计算题
(1)矿泉水中往往含多种有益于人体健康的成分。右图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥ ▲ mol。
(2)现代生活离不开铝,工业上以铝土矿为原料生产铝。
现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500 mL溶液。取
100 mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子)。
已知部分离子的物质的量浓度为:
c(H+) =" 0.02" mol·L-1 c(Mg2+) = 0.01 mol·L-1
c(Fe3+)=" 0.02" mol·L-1 c(Cl-) =" 0.52" mol·L-1
①溶液中Al3+物质的量浓度为 ▲ mol·L-1k*s5*u
②则该铝土矿样品中Al2O3的质量为 ▲ g(精确至0.01 g)。
查看答案和解析>>
科目:高中化学 来源:2013届浙江省宁波市高一上学期期末考试化学试卷 题型:计算题
(1)矿泉水中往往含多种有益于人体健康的成分。右图是某品牌矿泉水中标签上的部分内容,则这瓶矿泉水中含Ca2+的物质的量≥ ▲ mol。
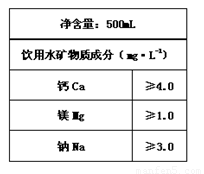
(2)现代生活离不开铝,工业上以铝土矿为原料生产铝。
现将一定量某铝土矿样品(主要成分Al2O3)溶于过量稀盐酸并制成500 mL溶液。取
100 mL该溶液,测得其中含有H+、Cl-、Mg2+、Al3+、Fe3+五种离子(不考虑其它离子)。
已知部分离子的物质的量浓度为:
c(H+) = 0.02 mol·L-1 c(Mg2+) = 0.01 mol·L-1
c(Fe3+)= 0.02 mol·L-1 c(Cl-) = 0.52 mol·L-1
①溶液中Al3+物质的量浓度为 ▲ mol·L-1k*s5*u
②则该铝土矿样品中Al2O3的质量为 ▲ g(精确至0.01 g)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com