
下表是不同温度下水的离子积常数:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | KW | 1×10-12 |
(1) > 因为水的电离是吸热反应,温度升高,水的电离程度增大,离子积也增大
(2) 7 (3) 碱性 > (4)酸性 <
解析试题分析:(1)水的电离过程是一个吸热过程,因此,升高温度,促进电离,相应的水的离子积常数也随之增大。
(2)25℃下水的离子积常数为1×10-14,则pH=13的氢氧化钠溶液与pH=1的稀盐酸等体积混合,所得混合溶液的pH为7.
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后所得溶液的溶质为CH3COONa,为强碱弱酸盐,其对应的溶液显碱性。由于CH3COO-的水解,因此c(Na+)>c(CH3COO-)。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后所得溶液溶质为CH3COOH、CH3COONa。且c(CH3COOH)>c(CH3COONa),溶液显酸性,由于溶液中CH3COOH的电离,因此c(Na+)<c(CH3COO-)。
考点:电解质溶液;水的电离
点评:本题所考查的都是基础题,熟练掌握课本的基础内容即可很好的解答。此题中应注意一个问题:“pH=3的醋酸”中由于醋酸是弱酸,因此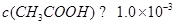 。
。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
| SO | 2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | t1 | t2 |
| Kw/mol2?L-2 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | KW | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | KW | 1×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com