
某有机物4.6克,完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重5.4克与8.8克,该有机物可能是( )
A、CH4 B、C2H4 C、C2H6 D、C2H6O
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al2Cl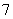 和AlCl
和AlCl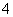 组成的离子液体作电解液时,可在钢制品上电镀铝。
组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品接电源的________极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为__________________________________________。若改用AlCl3水溶液作电解液,则阴极产物为________。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为________mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有________。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,______________(填“能”或“ 不能”)说明固体混合物中无Fe2O3,理由是________(用离子方程式说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知室 温下,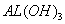 的K,或溶解度远大于
的K,或溶解度远大于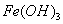 。向浓度均为0.1
。向浓度均为0.1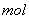

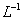 的
的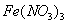 和
和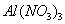 混合溶液中,逐滴加入NaOH 溶液。下列示意图表示生成
混合溶液中,逐滴加入NaOH 溶液。下列示意图表示生成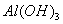 的物质的量与加入NaOH溶液的体积的关系 。合理的是
的物质的量与加入NaOH溶液的体积的关系 。合理的是
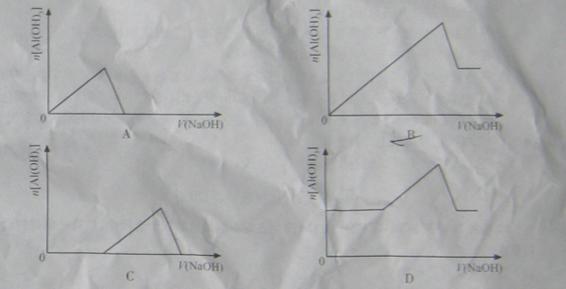
查看答案和解析>>
科目:高中化学 来源: 题型:
四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y
A.②③正确 B.只有③正确 C.①②③④正确 D.①②③正确
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴衣服上沾有动、植物油污,用水洗不掉,但可用汽油洗去,这是因为大多数有机物难溶于
而易溶于 。有机化工厂附近严禁火种,这是因为绝大多数有机物 。
⑵聚氯乙烯是一种 (填“有”或“无”)毒塑料,工业上用乙炔(CH≡CH)和氯化氢在催化剂作用下发生反应制取氯乙烯,氯乙烯再经过 反应制取聚氯乙烯。
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年4月22日是第44个“世界地球日”,主题是: “善待地球——科学发展”。下列行为中不符合这一主题的是
A、采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B、大量开采化石原料,以满足社会对能源的需求
C、减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D、节约能源,提高能源利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应原理的发展在化学的发展史上有重要的推动作用。
(1)用纯净的CaCO3与稀盐酸反应制取CO2气体,请回答:
实验过程如下图所示,分析判断________段化学反应速率最快,
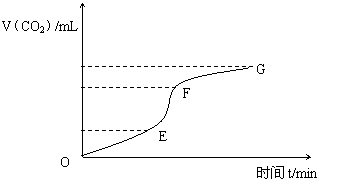
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)下面是一些常见分子的比例模型。其中1个分子中含有共用电子对最多的是 ( )
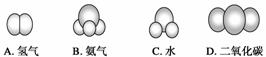
 (4)
(4)
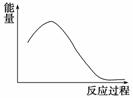
I.20世纪30年代,Eyring和Pzer提出化学反应的过渡态理论:化学反应在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 ________(填“吸热”或“放热”)反应。
II.在某体积为2 L的密闭容器中充入0.5 mol NO2和1 mol CO,在一定条件下发生反应:NO2+CO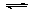 C O2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
C O2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速率为________________。
②下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是________________(填字母序号)。
A.容器内气体的质量保持不变
B.NO2的物质的量浓度不再改变
C.NO2的消耗速率与CO2的消耗速率相等
D.容器内气体的物质的量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq) PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K=
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化。在 溶液中PbSO4转化率较大,理由是
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],它和PbCO3受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO4)的成分提出如下假设。请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二: ;
假设三: 。
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成下表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥, |
②定量研究:取26.7 mg的干燥样品,加热,测
得固体质量随温度的变化关系如下图。某同学
由图中信息得出结论:假设一不成立。你是否
同意该同学的结论,并简述理由:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com