
| ������ | K+��Ag+��Mg2+��Ba2+ |
| ������ | NO3��CO32-��SO42-��SiO32- |
| ��� | ʵ������ | ʵ���� |
| �� | �����Һ�м�������ϡHCl | ������ɫ�������ų�0.56L���� |
| �� | ����ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ��������ù������� | ��������Ϊ2.4g |
| �� | �ڢ����Һ�еμ�BaCl2��Һ | ���������� |
���� �����⡰��ҺΪ������Һ����֪����Һ�к��е�����һ���ܹ��������棻��ʵ����֪������Һ��һ������CO32-����Ũ��Ϊ$\frac{\frac{0.56L}{22.4L/mol}}{0.1L}$=0.25mol/L����һ��û��Ag+��Mg2+��Ba2+�������ɰ�ɫ�����ж���Һ��һ������SiO32-��������ӦSiO32-+2H+=H2SiO3����������ȷֽ����ɶ������裬��������Ϊ2.4gΪ������������������ݹ�ԭ���غ㣬SiO32-��Ũ��Ϊ��$\frac{\frac{2.4g}{60g/mol}}{0.1L}$=0.4mol/L��
��ʵ����֪��Һ�в���SO42-�����ݵ���غ�2c��CO32-��+2c��SiO32-��=2��0.25mol/L+2��0.4mol/L=1.3mol/L��0.5mol/L�������Һ��һ������K+������Ũ������Ϊ0.8mol/L������ȷ��NO3-�Ƿ���ڣ��Դ˽����⣮
��� �⣺��1����ʵ����֪����������ϡ�������ɰ�ɫ�������ڱ�״���·ų�0.56L���壬�����Һ��һ������CO32-��SiO32-����һ��û��Ag+��Mg2+��Ba2+��
�ʴ�Ϊ��Ag+��Mg2+��Ba2+��
��2���������ᣬ�����ɰ�ɫ�����ж���Һ��һ������SiO32-��������ӦSiO32-+2H+=H2SiO3�����ʴ�Ϊ��SiO32-+2H+=H2SiO3����
��3���������ϼ����֪������ȷ��NO3-��c��CO32-��=0.25mol/L��c��SiO32-��=0.4mol/L��һ����������������ӣ�����c��SO42-��=0���ʴ�Ϊ��
| ������ | NO3- | CO32- | SiO32- | SO42- |
| c/mol•L-1 | �� | 0.25mol/L | 0.4mol/L | 0 |
���� ���⿼�����ӹ��桢���Ӽ����֪ʶ��Ϊ�߿��������ͣ��Ѷ��еȣ�ע���������ӷ�Ӧ��Ӧ�������������ӵļ��鷽�������ݵ���غ��ж�K+�Ƿ���ڣ��DZ�����ѵ㡢�״��㣮


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ֹ���ַ��� | B�� | ��ֹ��Ⱦ��� | C�� | �����к����� | D�� | ��ֹ��۱�ը |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | NaClO | C�� | KMnO4 | D�� | M2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
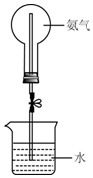 ijѧϰС���о���������Ȫʵ�飮
ijѧϰС���о���������Ȫʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
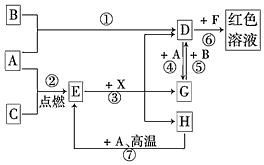 A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬BΪҺ�壬CΪ���壮D��E��F��G��H��X��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�壮����֮���ת����ϵ��ͼ��ʾ������ijЩ��Ӧ�����Ͳ��ַ�Ӧ������ȥ����
A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬BΪҺ�壬CΪ���壮D��E��F��G��H��X��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�壮����֮���ת����ϵ��ͼ��ʾ������ijЩ��Ӧ�����Ͳ��ַ�Ӧ������ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
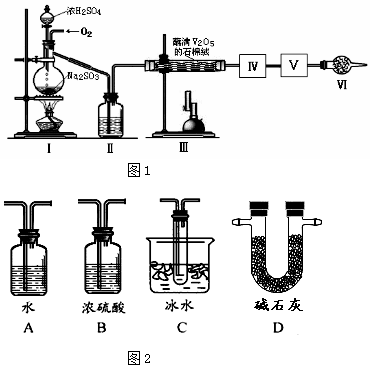
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��pH�Ʋⶨ���ȣ�����ΪpHΪ1��13 | |
| B�� | ����NaHCO3��ĩ����������CO2 | |
| C�� | ������Ƭ��һ��������H2 | |
| D�� | ����NaOH��Һ��-lg[OH-]һ����С |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com