
����� ÿƬ������������ ����Ӧ֢�� ����ȱ����ƶѪ֢��Ԥ���������� �������÷��� ����Ԥ���� �����ء� �ܹ⡢�ܷ⡢�ڸ��ﴦ���� |
(1)��ҩƷ��Fe2+�Ỻ�����������ҹ涨��ҩ����Fe2+�������ʳ���10.00%�������ٷ��á�
��Ϊ�˼���ijҩ����۵ġ������ơ��Ƿ�������ʵ����Ӧѡ�õļ����Լ�Ϊ__________(���Լ�������)��
��ʵ���ҿɲ���H2SO4�ữ��KMnO4��Һ���ԡ������ơ��е�Fe2+���еζ�(����ҩƷ�У������ɷֲ���KMnO4��Ӧ)������ƽ�������ӷ���ʽ��
__________![]() +__________Fe2++__________H+
+__________Fe2++__________H+![]() __________Mn2++__________Fe3++__________H2O
__________Mn2++__________Fe3++__________H2O
�۳�����������Ԫ����������Ϊ20.00%�ġ������ơ�
(2)��֪������������Է�������Ϊ172��������Ϊ�л��ᡣ��
(1)�����軯����Һ
��1��5��8����1��5��4
�۲����� n(Fe2+)=0.01 mol��L-1��12.00��10
m(Fe2+)=0.03 mol��
(
(2)HOOC��CH2��CH2��COOH+2NaOH![]() NaOOC��CH2��CH2��COONa+2H2O
NaOOC��CH2��CH2��COONa+2H2O
FeC4H4O4
������(1)��
KMnO4 �� 5Fe2+
1 5
0.01 mol��L-1��12.00 mol c(Fe2+)��20.00 mol
�ã�c(Fe2+)=0.03 mol��L-1
1 000 mL��Һ�к�Fe2+ 0.03 mol��
��ҩƷ��Fe2+��������Ϊ![]() ��100%=16.00%��10.00%�����Բ����Է���.
��100%=16.00%��10.00%�����Բ����Է���.
(2)��������ΪһԪ��ʱ������Է�������Ϊ![]() =59���������л������ԭ��.��������Ϊ��Ԫ��ʱ������Է�������Ϊ59��2=118���������������������λ�ò�ͬ����ԭ�ӣ�����������Ľṹ��ʽΪHOOC��CH2��CH2��COOH�������������Ļ�ѧʽΪC4H4O4Fe(��FeC4H4O4).
=59���������л������ԭ��.��������Ϊ��Ԫ��ʱ������Է�������Ϊ59��2=118���������������������λ�ò�ͬ����ԭ�ӣ�����������Ľṹ��ʽΪHOOC��CH2��CH2��COOH�������������Ļ�ѧʽΪC4H4O4Fe(��FeC4H4O4).


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

- 4 |
| 1000.00 mL |
| 20.00 mL |
| 10 g��20.00%-1.68 g |
| 10 g��20.00% |
| 1000.00 mL |
| 20.00 mL |
| 10 g��20.00%-1.68 g |
| 10 g��20.00% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㶫ģ�� ���ͣ��ʴ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
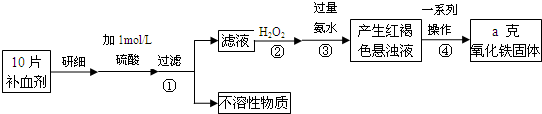
�������岻��ȱ�ٵ���Ԫ�أ����뺬���Ļ�����ɲ��������������ơ����г���һ�ֳ����IJ���ҩƷ���±���˵����IJ������ݡ���.��.��.Դ.��
| [���]ÿƬ������������ [��Ӧ֢]����ȱ����ƶѪ֢��Ԥ���������á� [�����÷�]����Ԥ���� С������Ԥ���� [����]�ܹ⡢�ܷ⡢�ڸ��ﴦ���档 |
(1) ��ҩƷ��Fe2+�Ỻ�����������ҹ涨��ҩ����Fe2+�������ʣ��Ѿ�������Fe2+��������Fe2+�������ı�ֵ������10.00% �������ٷ��á�
��ʵ���ҿɲ���H2SO4�ữ��KMnO4��Һ���ԡ������ơ��е�Fe2+���еζ�(����ҩƷ�������ɷݲ���KMnO4��Ӧ)����д���÷�Ӧ�����ӷ���ʽ��
��ʵ��ǰ������Ҫ��ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250 mL������ʱ��Ҫ�IJ������������������ձ�����ͷ�ι��⣬���� ��
��ijͬѧ��������еζ���ʽ���гֲ�����ȥ������������� ��������ĸ��ţ�

(2) ������������Ԫ����������Ϊ20.00%�ġ������ơ�10.00 g ������ȫ������ϡH2SO4�У����Ƴ�1000 ml��Һ��ȡ��20.00 ml����0.01000 mol•L-1��KMnO4��Һ�ζ�����ȥKMnO4��Һ12.00 ml ����ҩƷ��Fe2+��������Ϊ ��
(3) ��֪������Ϊ��Ԫ�л����ᣬ��23.6 g ���������Һ��4.0 mol•L-1 100.0 ml������������Һǡ����ȫ�к͡��˴Ź�����������ʾ�������������ͼ��ֻ���������շ塣д����������Һ������������Һ��ȫ�к͵Ļ�ѧ����ʽ(�л���д�ṹ��ʽ)
��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com