
双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN,其中N为-3价),化学方程式为:KCN + H2O2 + H2O = KHCO3 + A↑(已配平)
(1)生成物A的化学式为 。
(2)反应中被氧化的元素为 ,此反应中的氧化剂是 。
(3)用双线桥法表示该反应中电子转移的方向和数目:
(4)若有0.5molA生成,则转移的电子的物质的量为 mol。
 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源:2015-2016学年河北成安一中、永年二中高一上期中联考化学试卷(解析版) 题型:实验题
某同学设计如下实验方案,以分离NaCl和CaCl2两种固体混合物,试回答:
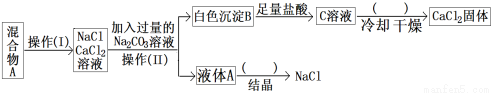
(1)操作I的名称是 ,操作II的名称是 。图中括号内的操作步骤均为 ;
(2)写出生成B的方程式为: 。
(3)按此实验方案得到的NaCl固体中肯定含有 (填化学式)杂质;为了解决这个问题可以向操作(II)得到的液体A中加入适量的 ;反应的方程式为:__________________;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(文)化学试卷(解析版) 题型:选择题
鉴别织物成分是真丝还是人造丝,正确的操作方法是
A.滴加醋酸 B.滴加浓硫酸 C.滴加酒精 D.灼烧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上学期期中理综化学试卷(解析版) 题型:填空题
一定条件下,在体积为3 L的密闭容器中反应:CO(g)+ 2H2(g)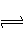 CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
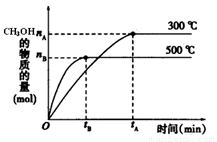
(1)根据右图,升高温度,K值将 (填“增大”、“减小”或“不变”)。
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是 (用nB、tB表示)。
(3)该可逆反应达到化学平衡状态的标志是 (填字母)。
a、CO、H2、CH3OH的浓度均不再变化
b、混合气体的密度不再改变
c、混合气体的平均相对分子质量不再改变
d、v生成(CH3OH)= v消耗(CO)
(4)300℃时,将容器的容 积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母)。
积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母)。
a、c(H2)减少 b、正反应速率加快,逆反应速率减慢
c、CH3OH 的物质的量增加 d、重新平衡时c(H2)/ c(CH3OH)减小
(5)根据题目有关信息,请在右下坐标图中标示出该化学反应过程的能量变化(标明信息)。
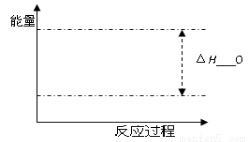
(6)以甲醇、空气、氢氧化钾溶液为原料, 石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,该电池中负极上的电极反应式是:
石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,该电池中负极上的电极反应式是:
2CH3OH–12e-+16OH-= 2CO32-+ 12H2O ,则正极上发生的电极反应为: 。
查看答案和解析>>
科目:高中化学 来源:2016届四川省资阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:填空题
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
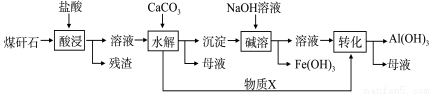
(1)“酸浸”过程中主要反应的离子方程式为:_____________、_____________。
(2)“酸浸”时,提高浸出速率的具体措施有_____________、_____________。(写出两个)
(3)“碱溶”的目的是_____________。物质X的化学式为_____________。
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:_____________。
(5)若根据过滤出的Fe(OH)3沉淀来推算煤矸石中Fe2O3 的含量,须将沉淀清洗干净,检验沉淀是否洗干净的具体操作方法是_______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中测试化学试卷(解析版) 题型:选择题
常温常压下,用等质量的 CH4、CO2、O2、SO2 分别吹出四个气球(如下图),其中气体为CH4的是
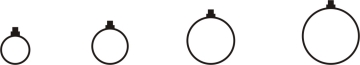
A B C D
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三11月月考理科综合化学试卷(解析版) 题型:填空题
锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为6C+xLi++xe- = LixC6。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
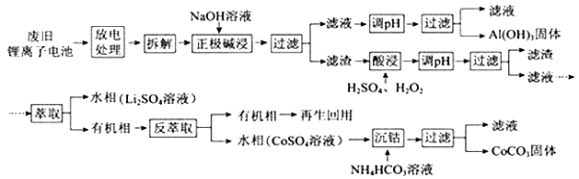
回答下列问题:
(1)LiCoO2中,Co元素的化合价为 。
(2)写出“正极碱浸”中发生反应的离子方程式 。
(3)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式 ;可用盐酸代替H2SO4和H2O2的混合液,但缺点是 。
(4)写出“沉钴”过程中发生反应的化学方程式 。
(5)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池反应方程式 。
(6)上述工艺中,“放电处理”有利于锂在正极的回收,其原因是 。在整个回收工艺中,可回收到的金属化合物有 (填化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列化学方程式中,不能用离子方程式H++OH-=H2O表示的是
A.2NaOH + H2SO4 = Na2SO4 + 2H2O
B. Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
C.Ba(OH)2 + 2HCl = BaCl2 + 2H2O
D.KOH + HCl = KCL + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com