
(07年江苏卷)一定温度下可逆反应:A(s)+2B(g)![]() 2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是()
2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是()
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增大
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
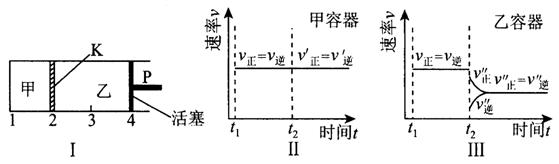
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
答案:BD
考点:本题考查了勒夏特列原理的应用、化学平衡图像知识。
解析:由题给反应可知A是固体,该反应正反应是气体分子数增大的反应。甲容器加入1molA和2molB,乙容器加入4molC和2molD,完全转化后得2molA和4molB,乙的体积是甲的2倍,两者起始建立等效平衡。A项中,再在甲中加入1molA和2molB,相当于在起始加入2molA和4molB,由于甲体积比乙小,甲中压强加大,平衡向逆反应方程式移动,甲中C的浓度小于乙中C的浓度的2倍,A不正确。B中温度升高,平衡向逆反应方向移动,B的体积分数均增大。C中使甲、乙两容器体积相等,乙中投入量相当于甲的2倍,乙中压强增大(类似于选项A),平衡向逆反应方向移动,乙中C的体积分数小于甲C的体积分数的2倍。D中,甲容器中总压强增大,但反应物和生成物的浓度不变,速率不发生变化,平衡不发生移动,图2正确。乙容器中保持恒压,体积增大,浓度减小,正、逆反应速率都减小,体积增大,平衡向正反应方向移动,逆反应速率大于正反应速率,图3正确。


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
(07年江苏卷)下列说法正确的是()
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
A.除去铁粉中混有的少量铝粉.可加人过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
(07年江苏卷) 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= + 49.0 kJ?mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ?mol-1
下列说法正确的是()
A.CH3OH的燃烧热为192.9 kJ?mol-1
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应: CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
(07年江苏卷) 阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是()
A.2.24LCO2中含有的原子数为0.3 ×6.02×1023
B.0.1L3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3 ×6.02×1023
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D.4.5 SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com