
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列叙述错误的是

A. T的氧化物能与碱反应
B. 元素的非金属性:Q强于W
C. W的单质共热时,能与其最高价氧化物的水化物浓溶液反应
D. 原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】2014年7月21日,世界各国领导人在南非德班共同商讨应对气候变化的道路—“拯救人类的最后机会”。要想节能减排下列属最有希望的新能源是( )
①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能
A.①②③④B.⑤⑥⑦⑧C.③④⑤⑥D.除①②③外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示装置和原理能达到目的的是 ( )
注:H2C2O4·2H2O的熔点为101 ℃,170 ℃以上分解;CaO2在350 ℃以上分解。
A. 制取氨气 B. 碳酸氢钙的分解
B. 碳酸氢钙的分解 C. CaO2分解成CaO、O2
C. CaO2分解成CaO、O2 D. 草酸的分解
D. 草酸的分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向 100mL Na2CO3 与 NaAlO2 的混合溶液中逐滴加入 1mol/L 的盐酸,测得溶液中的 CO32-、HCO3- 、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。下列说法正确的是

A. 原 混 合 溶 液 中 的 n (CO32-): n (AlO2-)=2:1
B. a 点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-)
C. b 点溶液中离子浓度顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH- )
D. d→e 的过程中水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中字母分别代表一种元素。回答下列问题。
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | a | b | c | d | ||||
3 | e | f | g | x | y | z |
(1)表中所标元素,最活泼的金属元素形成简单离子符号为____;最不活泼的元素的原子结构示意图为 _____;其中一种元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该盐是_______。
(2)写出两种满足下列条件的物质______(写化学式)。
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是______(填化学式)。
(4)表中元素的最高价氧化物的水化物中:酸性最强的是______(填化学式,下同);碱性最强的是_______,这两种物质反应的离子方程式为_________。
(5)推测元素的非金属性:a ______ g(填“>”或“<”)。利用图装置设计实验,证明推测结论。
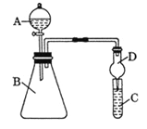
①仪器A的名称为___________,干燥管D的作用是______________。
②填空。
装置内试剂 | C中发生反应的化学方程式 | ||
A | B | C | |
稀硫酸 | 碳酸钠 | _______ | _______ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. 氨水中通入少量的SO2气体: SO2+ OH- == HSO3-
B. 氯气与水的反应: Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C. 氯化钙溶液中通入CO2气体: Ca2++H2O+CO2== CaCO3↓+2H+
D. 二氧化锰跟浓盐酸共热制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池构造如图所示。下列有关叙述正确的是( )

A. 在外电路中,电子由银电极流向铜电极
B. 取出盐桥后,电流计的指针仍发生偏转
C. 外电路中每通过0.2mol电子,铜的质量理论上减小12.8g
D. 原电池的总反应式为Cu +2AgNO3 ==== 2Ag +Cu(NO3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com