确定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A通常显______价,A的电负性______B的电负性;
A的第一电离能______B的第一电离能(填“>”、“<”或“=”).
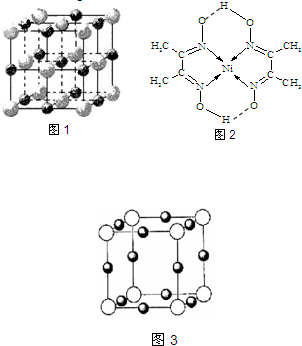
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示,其中TiN中N呈-3价),已知3种离子晶体的晶格能数据如下表:
| 离子晶体 | KCl | MgO | CaO |
| 晶格能/kJ?mol-1 | 715 | 3791 | 3401 |
则该 4种离子晶体熔点从高到低的顺序是:______.其中MgO晶体中一个Mg
2+周围和它最邻近且等距离的Mg
2+有______个.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V
2O
5和CrO
2中,适合作录音带磁粉原料的是______.
(4)某配合物的分子结构如图2所示,其分子内不含有______(填序号).
A.离子键 B.极性键 C.金属键
D.配位键 E.氢 键 F.非极性键
(5)某离子X
+中所有电子正好充满K、L、M三个电子层,它与N
3-形成的晶体结构如右图所示.X的元素符号是______,与同一个N
3-相连的X
+有______个.
(6)在硼酸[B(OH)
3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构.则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是______
A.SP,范德华力 B.sp
2,范德华力 C.sp
2,氢键 D.sp
3,氢键
(7)CaC
2中

与

互为等电子体,

的电子式可表示为______;1mol

中含有的π键数目为______.


 与
与 互为等电子体,
互为等电子体, 的电子式可表示为______;1mol
的电子式可表示为______;1mol  中含有的π键数目为______.
中含有的π键数目为______.
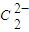 与
与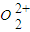 、N2都互为等电子体,根据氮气分子的电子式写出
、N2都互为等电子体,根据氮气分子的电子式写出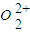 的电子式,根据每个
的电子式,根据每个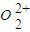 中的π键个数计算1mol
中的π键个数计算1mol 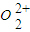 中含有的π键数目.
中含有的π键数目.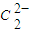 与
与 、N2都互为等电子体,由氮气分子的电子式知
、N2都互为等电子体,由氮气分子的电子式知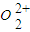 的电子式为
的电子式为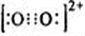 ,每个
,每个 中含有2个π键,所以1mol
中含有2个π键,所以1mol 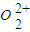 中含有的π键数目是2NA,
中含有的π键数目是2NA, ;2NA.
;2NA.

 全能测控一本好卷系列答案
全能测控一本好卷系列答案 (3)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图一所示),其中3种离子晶体的晶格能数据如下表:
(3)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图一所示),其中3种离子晶体的晶格能数据如下表: (2013?渭南二模)决定物质性质的重要因素是物质结构.请回答下列问题.
(2013?渭南二模)决定物质性质的重要因素是物质结构.请回答下列问题. 确定物质性质的重要因素是物质结构.请回答下列问题.
确定物质性质的重要因素是物质结构.请回答下列问题.