
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成OCN-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
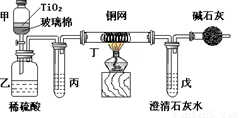
(1)乙中反应的离子方程式为 。
(2)乙中生成的气体除N2和CO2外,还有副产物HCl及Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是___________(填字母)
A.饱和食盐水 B.饱和NaHCO3溶液 C.浓NaOH溶液 D.浓硫酸
(3)丁在实验中的作用是 。
装有碱石灰的干燥管的作用是 。
(4)戊中盛有含Ca(OH)2 0.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于 。若该测得值与实际处理的百分率相比偏低,请简要说明可能的任意一个原因 。
(5)请提出一个能提高准确度的建议(要有可操作性,不宜使操作变得过于复杂) 。
(1)2CNO-+2H++3ClO-=N2↑+ 2CO2↑+3Cl-+H2O;
(2)A
(3)除去氯气 止空气中的二氧化碳进入戊装置,对实验产生影响
(4)0.82 氧化碳吸收不完全,可能有装置中滞留有CO2;戊中CO2流速过快,吸收不完全等;
(5)不将甲中溶液一次加入,改为分次加入,控制二氧化碳产生速率或乙中增加一根导管,反应结束后通入除去二氧化碳的空气,排尽装置中的二氧化碳或澄清石灰水改成氢氧化钠溶液,测定增重,也可加入石灰水测沉淀质量。
【解析】
试题分析:(1)根据提供的反应物和产物,书写离子方程式为2CNO-+2H++3ClO-=N2↑+ 2CO2↑+3Cl-+H2O;
(2)装置丙的作用是除去HCl,选用饱和食盐水;
(3)实验的目的是得到二氧化碳的量,杂质气体均要除去,丁用金属铜除去氯气;为防止空气中的二氧化碳进入戊装置,对实验产生影响,故加一个干燥管隔离空气;
(4)根据数值知石灰水过量,n(CN-)=n(CO2)=n(CaCO3)=0.82÷100=0.0082mol
CN-被处理的百分率为0.0082÷(0.2×0.05)=0.82
该测得值与实际处理的百分率相比偏低的原因是二氧化碳吸收不完全,可能有装置中滞留有CO2;戊中CO2流速过快,吸收不完全等;
(5)不将甲中溶液一次加入,改为分次加入,控制二氧化碳产生速率或乙中增加一根导管,反应结束后通入除去二氧化碳的空气,排尽装置中的二氧化碳或澄清石灰水改成氢氧化钠溶液,测定增重,也可加入石灰水测沉淀质量。
考点:考查化学实验中实验操作、实验目的、计算及实验分析等有关问题。


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
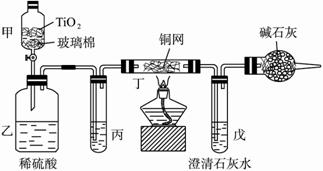
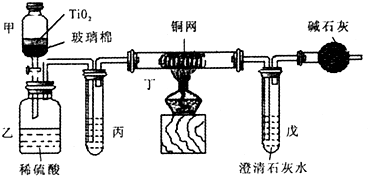
将浓缩后含CN -的污水与过量NaClO溶液的混合液共200 mL(其中CN -的浓度为0.05 mol· L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:?
(1)甲中反应的离子方程式为 ,?
乙中反应的离子方程式为 。
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是。 (填字母)?
a.饱和食盐水 b.饱和NaHCO3溶液? c.浓NaOH溶液 d.浓硫酸?
(3)丁在实验中的作用是 ,?
装有碱石灰的干燥管的作用是 。?
(4)戊中盛有含Ca(OH)2 0.02 mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于 。?
请说明该测得值与实际处理的百分率相比偏高还是偏低 ?简要说明可能的原因 。?
(5)请提出一个能提高准确度的建议(要有可操作性,不宜使操作变得过于复杂) 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年广西省高三上学期第三次月考化学试卷 题型:实验题
(14分)电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。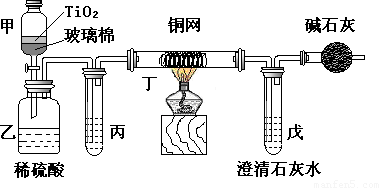
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
⑴乙中反应的离子方程式为______________ ___________。
⑵乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
⑶丁在实验中的作用是_____ __________________ ,
装有碱石灰的干燥管的作用是___________ ___________。
⑷戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液200 mL(其中CN-的浓度为0.05 mol?L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。
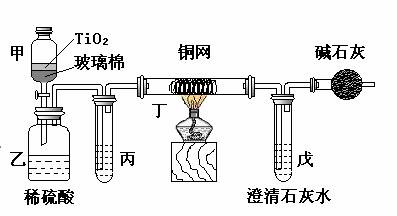
(1) 甲中反应的离子方程式为_______________;乙中反应的离子方程式为________
(2) 乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。丙中加入的除杂试剂是____________(填字母)
a.饱和食盐水 b.饱和NaHCO3溶液
c.浓NaOH溶液 d.浓硫酸
(3)丁在实验中的作用是__________________________________
(4)戊中盛有足量的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于_________________。请说明该测得值与实际处理的百分率相比偏高还是偏低?简要说明理由______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com