
| A、Na2S;Na2O;Na2SO3 |
| B、Na2SO4;Na2O;Na2SO3 |
| C、Na2O;Na2S;Na2SO4 |
| D、Na2S;Na2SO4;Na2SO3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X肯定为碱金属元素 |
| B、稳定性:Y的氢化物>Z的氢化物 |
| C、X、Y两元素形成的化合物可能为离子晶体 |
| D、Y、Z两元素形成的化合物熔点较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第七周期排满时有32种元素,全部是放射性元素 |
| B、第七周期排满时最后一种单质不与任何物质发生化学反应 |
| C、第七周期第ⅦA族元素的原子序数为117,是一种金属 |
| D、第七周期第ⅢA族元素的氢氧化物与Al(OH)3具有相似的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Fe和足量Cl2反应转移的电子数为2NA |
| B、标况下,11.2LCH4和C2H4混合气体中含氢原子数为2NA |
| C、标准状况下,22.4 L 氖气中含氖原子数为2NA |
| D、在1L 0.1 mol?L-1Na2SO4溶液中含离子数:Na+ 0.2 NA、SO42- 0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
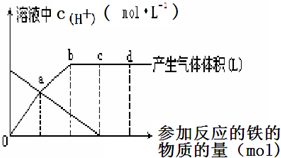 铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )
铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )| A、0点到a点的还原产物是NO |
| B、因反应放热,使溶液温度升高,a点到b点的还原产物是N2O |
| C、反应过程到达b点时HNO3已完全反应 |
| D、c点和d点参加反应的铁的物质的量之比是2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙>甲>乙 |
| B、甲=丙>乙 |
| C、甲=乙=丙 |
| D、乙>丙>甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 实验要求 | 除去二氧化碳中少量的氧气 | 清洗金属表面油污 | 检验石灰中是否含有石灰石 | 区分黄铜(铜锌合金)和黄金 |
| 第一方案 | 通过灼热炭粉 | 用洗洁精洗涤 | 加热 | 观察颜色 |
| 第二方案 | 通过灼热铜丝网 | 用水洗涤 | 滴加醋酸 | 加盐酸,看气泡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com