
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂,又不作还原剂的是
A.Na2O+H2O=2NaOH B.2F2+2H2O=4HF+O2
C.3NO2+H2O=2HNO3+NO D.2Na+2H2O=2NaOH+H2↑
科目:高中化学 来源: 题型:
【题目】如图,烧瓶中充满a气体,滴管和烧杯中盛放足量b溶液,将滴管中溶液挤入烧瓶,打开止水夹f,能形成喷泉的是( )
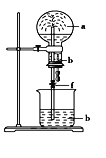
A. a是Cl2,b是饱和NaCl溶液
B. a是NO,b是H2O
C. a是 NH3,b是稀盐酸溶液
D. a是CO2,b是H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出化学方程式或离子方程式:
(1)乙酸乙酯和氢氧化钠溶液共热的化学方程式 .
(2)工业制粗硅的化学方程式 .
(3)偏铝酸钠溶液中通入过量二氧化碳的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研单位利用电化学原理用SO2来制备硫酸,装置如下图,含有某种催化剂。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
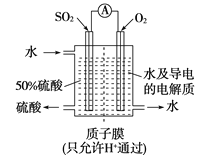
(1)通入SO2的电极为__________极,其电极反应式为_________________,此电极区pH_______(填“增大”“减小”或“不变”)。
(2)若通入SO2的速率为2.24 L/min(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率是 (结果用 mL/min表示)
(3)以此电源电解足量的硝酸银溶液,若阴极产物的质量为21.6 g,则阳极产生气体标准状况下体积为__________L。
(4)常温时,BaSO4的Ksp=1.08×10-10。现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为________。
(5)已知:Fe2O3(s)+3C(石墨)==2Fe(s)+3CO(g) ΔH =+489.0 kJ·mol-1
CO(g)+1/2O2(g)==CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)==CO2 (g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)==2Fe2O3(s)的ΔH为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中给CO和水蒸气的混合物加到800℃时,有下列平衡:CO+H2OCO2+H2且K=1,若用2molCO和10molH2O(气)相互混合并加热到800℃,达平衡时CO的转化率约为( )
A. 16.7% B. 50% C. 66.7% D. 83%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是:
A. 稀盐酸滴入硝酸银溶液中;Ag++Cl-=AgCl↓
B. 稀硝酸滴在碳酸钙上:CO32-+2H+=CO2↑+H2O
C. 稀硫酸滴在铜片上:Cu+2H+ = Cu2++H2↑
D. 氯气通入氯化亚铁溶液中:Fe2++Cl2 =Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯和氯乙烯相同点的说法不正确的是
A. 都属于有机物中的烃类 B. 都含有双键而具有不饱和性
C. 都可发生加聚反应 D. 都是重要的化工生产原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质甲放入显黄色的乙的浓溶液中,剧烈反应产生混合气体A,A在常温下不与空气作用,有如图变化关系:

(1)C的化学式为________。
(2)写出甲跟乙反应的化学方程式:______________________
(3)写出单质丙与乙的浓溶液反应的化学方程式:_________________
(4)写出单质丙与乙的稀溶液反应生成气体B的离子方程式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com