设NA 表示阿伏加德罗常数的值,下列说法正确的是( )
A.含1molHCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为2NA
B.100mL0.1mol?L-1的稀硫酸中含有SO42-个数为0.1NA
C.标准状况下,11.2LCCl4含有的分子数为0.5NA
D.含有0.1NA个CO32-的Na2CO3固体的质量为10.6g
【答案】
分析:A.根据反应Fe+2HCl=FeCl
2+H
2↑判断;
B.根据N=nN
A=cVN
A计算;
C.标准状况下,CCl
4为液体;
D.根据m=nM计算.
解答:解:A.由Fe+2HCl=FeCl
2+H
2↑反应可知,含1molHCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为N
A,故A错误;
B.N(SO
42-)=0.1L×0.1mol/LN
A=0.01N
A,故B错误;
C.标准状况下,CCl
4为液体,V
m≠22.4L/mol,故C错误;
D.n(Na
2CO
3)=n(CO
32-)=
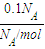
=0.1mol,m(Na
2CO
3)=0.1mol×106g/mol=10.6g,故D正确.
故选D.
点评:本题考查阿伏加德罗常数,题目难度不大,注意物质存在的状态以及物质的量的相关计算公式的运用.

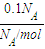 =0.1mol,m(Na2CO3)=0.1mol×106g/mol=10.6g,故D正确.
=0.1mol,m(Na2CO3)=0.1mol×106g/mol=10.6g,故D正确.
