
| A. | SiO2 | B. | CCl4 | C. | NaCl | D. | H2O |
科目:高中化学 来源: 题型:选择题
| A. | CH3CH | B. | CH2Cl2 | C. | CCl4 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| C. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 | |
| D. | 原混合溶液中FeBr2的物质的量为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
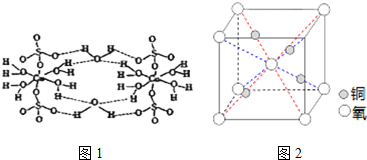
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第2周期与第3周期元素从左到右,最高正化合价均从+1逐渐增大至+7,0族元素一般是0价 | |
| B. | 3个长周期所含元素种数相同 | |
| C. | 不同主族的3、4周期元素原子序数的差可能不同 | |
| D. | 同周期从左到右,非金属元素含氧酸的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol组成为C2H6O的有机物,所含C-H键数目可能为0.5NA | |
| B. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA | |
| D. | 标准状况下,22.4 L HF所含的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温高压下,28gN2和6gH2充分反应生成NH3的分子数为2NA | |
| B. | 1mol/LFeCl3 溶液中所含Fe3+的数目小于NA | |
| C. | 常温下,1LpH=12的氨水中含OH-的数目为0.1NA | |
| D. | 23g NO2和N2O4的混合气体中含有氮原子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com