
下列热化学方程式中ΔH代表燃烧热(25℃,101 kPa)的是
A.CH4(g)+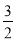 O2(g)
O2(g)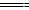 2H2O(l)+CO(g)ΔH1
2H2O(l)+CO(g)ΔH1
B.2CO(g)+O2(g)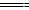 2CO2(g)ΔH2
2CO2(g)ΔH2
C.S(s)+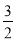 O2(g)
O2(g)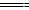 SO3(s)ΔH3
SO3(s)ΔH3
D.C6H12O6(s)+6O2(g)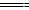 6CO2(g)+6H2O(l)ΔH4
6CO2(g)+6H2O(l)ΔH4
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA | |
| B. | 常温下,46 g分子式为C2H6O的物质中一定含有极性键为7NA,非极性键为NA | |
| C. | 125 mL 16 mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于NA | |
| D. | 标准状况下,体积为22.4 L NO2、N2O4的混合气体,升温至常温,则混合气体分子数为NA |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子.则该硫酸盐的物质的量浓度为
A.2 mol•L﹣1 B.7.5 mol•L﹣1 C.5 mol•L﹣1 D.2.5 mol•L﹣1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
隐形眼镜越来越受到年青人的喜爱,在使用隐形眼镜时,常用的护理药水中含有过氧化氢(H2O2).下列有关过氧化氢的说法中正确的是
A.过氧化氢是由氢气和氧气组成的
B.它是由2个氢元素和2个氧元素组成的
C.过氧化氢在二氧化锰作用下能生成水和氧气,该反应为复分解反应
D.每个过氧化氢分子中含有2个氢原子和2个氧原子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:选择题
已知1 mol白磷完全转化为红磷放出29.2 kJ热量,下列两个反应:P4(白,s)+5O2(g)=2P2O5(s)ΔH=-Q1,4P(红,s)+5O2(g)=2P2O5(s)ΔH=-Q2,Q1与Q2的关系是
A.Q1=Q2 B.Q1<Q2 C.Q1>Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:选择题
在化学反应A(g)+3B(g)  2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是
2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是
A.v(A)=v(B) B.v(A)=2v(C) C.3v(B)=v(C) D.v(B)=3v(D)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:填空题
(一题多变题组)关于物质的量各物理量之间的相互转化
(1)同温同压下,同体积的氨气(NH3)和硫化氢(H2S)气体的质量比为___________;同质量的氨气和硫化氢气体的物质的量比为_____________,所含原子个数比为__________;若两者所含氢原子数相等,它们的物质的量比是_____________。
(2)标准状况下,①4 g氢气、② 33.6 L甲烷、③ 6.02×10 23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。
23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。
(3)现有质量为a g某气体A2B,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:该气体的物质的量为_____ ___mol,该气体所含原子总数为___ ____个,该气体在标准状况下的体积为____________L。
(学法题)通过解答本题,在解题时应先将各种已知量转化为 再进行计算。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 3.48 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 1.58 | 158 |
| 硝酸银 | 0.02 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 消耗盐酸的体积/mL | 待测KOH溶液的体积/mL |
| 1 | 27.23 | 25.00 |
| 2 | 28.24 | 25.00 |
| 3 | 27.25 | 25.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com