
| A. | 1:1:1 | B. | 4:4:5 | C. | 5:5:4 | D. | 无法确定 |
分析 气体的体积相等,相同条件下气体的物质的量相等,令气体的物质的量为1mol,则烧瓶的容积为22.4L,确定溶质的物质的量,根据物质的量浓度公式计算判断:
①混有少量空气的HCl,HCl完全溶于水,溶液的体积等于HCl气体的体积;
②纯净的NO2气体,发生反应3NO2+H2O=2HNO3+NO,生成硝酸$\frac{2}{3}$mol,$\frac{1}{3}$molNO,所以溶液体积等于烧瓶容积的$\frac{2}{3}$;
③NO2与O2体积比4:1,NO2为$\frac{4}{5}$×1mol,发生反应4NO2+O2+2H2O=4HNO3,生成硝酸为$\frac{4}{5}$×1mol,溶液体积等于烧瓶容积.
解答 解:气体的体积相等,相同条件下气体的物质的量相等,令气体的物质的量为1mol,则烧瓶的容积为22.4L,
①混有少量空气的HCl,其中的HCl完全溶于水,溶液的体积等于HCl气体的体积,设HCl气体为xmol,则所得溶液的体积为22.4xL,所以溶液浓度为$\frac{xmol}{22.4xL}$=$\frac{1}{22.4}$mol/L;
②纯净的NO2气体,发生反应3NO2+H2O=2HNO3+NO,生成硝酸$\frac{2}{3}$mol,$\frac{1}{2}$molNO,所以溶液体积等于烧瓶容积的$\frac{2}{3}$,所以溶液的物质的量浓度为:$\frac{\frac{2}{3}mol}{\frac{2}{3}L}$=$\frac{1}{22.4}$mol/L;
③NO2为$\frac{4}{5}$×1mol,发生反应4NO2+O2+2H2O=4HNO3,生成硝酸为$\frac{4}{5}$×1mol,溶液体积等于烧瓶容积,所以溶液物质的量浓度为:$\frac{\frac{4}{5}mol}{22.4L}$=$\frac{1}{22.4}$×$\frac{4}{5}$mol/L;
所以实验后三个烧瓶中溶液的物质的量浓度之比为$\frac{1}{22.4}$mol/L:$\frac{1}{22.4}$mol/L:$\frac{1}{22.4}$×$\frac{4}{5}$mol/L=5:5:4,
故选C.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确反应后溶质组成及溶液体积为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 4:13 | B. | 1:13 | C. | 1:3 | D. | 13:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:C2H5OH | B. | C的基态原子核外电子轨道表示式: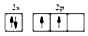 | ||
| C. | 氯化铵的电子式: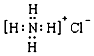 | D. | CS2分子比例(填充)模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | O2 | C. | H2O | D. | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
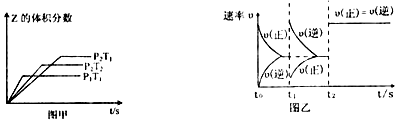
| A. | 图甲,P1>P2,a<3 | |
| B. | 图甲,T1<T2,Q>0 | |
| C. | 图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 | |
| D. | 图乙,如果a=3,t2时表示向体系中加入了催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝、氢氧化钠都是常见的胃酸中和剂 | |
| B. | 海轮外壳镶嵌锌块是利用牺牲阳极的阴极保护法 | |
| C. | 水泥、玛瑙、分子筛都是硅酸盐工业产品 | |
| D. | 明矾净水时的作用是杀菌、消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com