
下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A | 苯甲酸的溶解度随温度升高而增大 | 用蒸发浓缩、冷却结晶、过滤,除去苯甲酸中混有的泥沙 |
B | NH4Cl受热容易分解 | 加热NH4Cl制备NH3 |
C | SO2具有漂白性 | SO2能使酸性KMnO4溶液褪色 |
D | 某温度下,碳酸的K1=4.4×10-7,次氯酸的K=2.98×10-8 | 用CO2和NaClO溶液制备HClO |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于化学的叙述中,错误的是
A.在化工生产中应遵循“绿色化学”的思想
B.通常用来衡量一个国家的石油化学工业发展水平的标志是乙烯的产量
C.在元素周期表的金属和非金属分界线附近寻找半导体材料
D.根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:实验题
选考【化学——选修2:化学与技术】(15分)某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中舍有Ni70.0%及一定量的Al、Fe、SiO2和有机物,镍及其化台物的化学性质与铁的类似,但Ni2-的性质较稳定)。
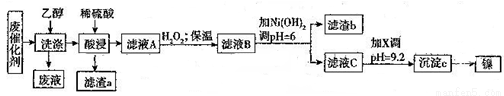
已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
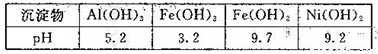
(1)滤渣a的成分是________,用乙醇洗涤废催化剂的目的是________,从废渣中回收乙醇的方法是________。
(2)为提高酸浸速率,可采取的措施有(答两条)________________。
(3)向A中加人 H2O2时反应的离子方程式为__________.试剂x可以是________。
(4)用方程式表示出由沉淀。制取单质镍的方法_________、________。回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了a kgNi(OH)2 ,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为________kg(填计算式)。
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应。
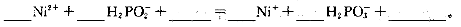
与电镀相比,化掌镀的最大优点是:________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
用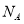 表示阿伏加德罗常数的值,下列叙述正确的是(Cu-64 O-16)
表示阿伏加德罗常数的值,下列叙述正确的是(Cu-64 O-16)
A.1mol Na2O2晶体中阴离子的个数为2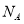
B.标准状况下,2.24L苯所含的分子总数为0.1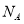
C.32gO2和32g O3的所含的氧原子数都是为2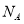
D.6.4g铜与过量的浓硝酸完全反应转移的电子数是0.1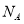
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:实验题
(16分)工业废渣、废水回收利用是重要研究课题。下面流程是生产食用香料正丁酸乙酯的工厂废水(含乙醇、正丁酸乙酯、正丁酸、乙醚和大量无机悬浮物)联合利用电子工业废料(含SiO2和Cu2(OH)2CO3)回收铜的工艺设计。
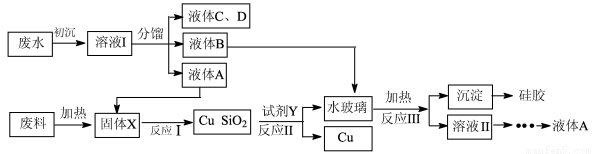
回答下列问题:
(1)初沉加入的试剂是明矾,写出参与净水的离子的水解方程式: 。
(2)固体X的成分是 ,反应I的化学反应方程式 。
(3)试剂Y为 ;加快反应II速率的措施有(任写一条) 。
(4)反应Ⅲ的离子方程式为: 。
(5)硅胶在生活与生产中用途广泛,写出其中一种用途 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:选择题
下列各组离子能在溶液中大量共存的是
A.Fe3+、K+、Br 、SCN
、SCN B.NH
B.NH 、Na+、CO
、Na+、CO 、OH
、OH
C.K+、Na+、PO 、NO
、NO D.Al3+、Mg2+、SO
D.Al3+、Mg2+、SO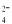 、HCO
、HCO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:填空题
(12分)利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:
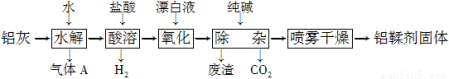
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90℃而不在室温下进行的原因是____。
(2)“酸溶”时,Al2O3发生反应的离子方程式为____。
(3)“氧化”时,发生反应的离子方程式为____。
(4)“废渣”成分为________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河北区高三总复习质量检测一化学试卷(解析版) 题型:实验题
(19分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
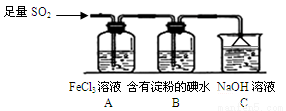
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 。
(2)装置C的作用是 。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯
E.玻璃棒
F.坩埚
(4)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成 ;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42—。该做法 (填“合理”或“不合理”),理由是 。
(5)能表明I-的还原性弱于SO2的现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古鄂尔多斯市高三模拟化学试卷(解析版) 题型:选择题
分析下列各项结构的规律,按此规律排布第10项的分子式应为
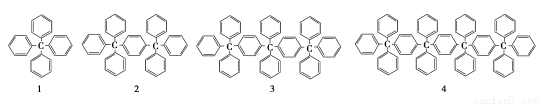
A.C198H146 B.C196H155 C.C196H146 D.C198H155
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com