火力发电厂产生大量的氮氧化物(NO
x)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NO
x:
CH
4(g)+4NO
2(g)=4NO(g)+CO
2(g)+2H
2O(g)△H
1=-574kJ?mol
-1CH
4(g)+4NO(g)=2N
2(g)+CO
2(g)+2H
2O(g)△H
2=-1160kJ?mol
-1甲烷直接将NO
2还原为N
2的热化学方程式为
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
.
(2)脱碳.将CO
2转化为甲醇的化学方程式为:
CO
2+3H
2
CH
3OH(g)+H
2O(g)
①取五份等体积CO
2和H
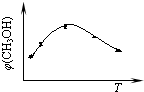
2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,tmin后,测得甲醇的体积分数φ(CH
3OH) 与反应温度T的关系曲线如图所示,则上述合成甲醇的反应的逆反应为
吸热
吸热
反应(填“放热”或“吸热”).
②在一恒温恒容密闭容器中充入1mol CO
2和3mol H
2,进行上述反应.测得CO
2和CH
3OH(g)的浓度
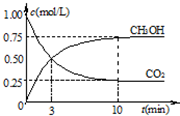
随时间变化如图所示.下列说法正确的是
CE
CE
A.10min后,向该容器中再充入1mol CO
2和3mol H
2,则再次达到平衡时c(CH
3OH)=1.5mol?L
-1B.0~10min内,氢气的平均反应速率为0.075mol?L
-1?min
-1C.达到平衡时,氢气的转化率为75%
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH
3OH)/n(CO
2)减小
③能说明CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)达到平衡状态的是
C
C
A.生成甲醇的速率与生成水的速率相等
B.v(H
2)=3v(CH
3OH)
C.恒容容器中,体系的压强不再改变
D.恒容容器中,混合气体密度不再发生改变
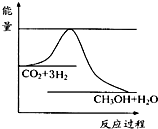
④右图表示反应CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)进行过程中能量(单位为kJ?mol
-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO
2和3mol H
2,达到平衡后,采取下列措施中能使c(CH
3OH)增大的是
CD
CD
.
A.使用新高效催化剂 B.充入He(g),使体系压强增大
C.将H
2O(g)从体系中分离出来 D.再充入1mol CO
2和3mol H
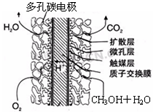
2⑤甲醇燃料电池结构如图所示,其工作时正极的电极反应式可表示为
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
.
(3)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.
硫酸铵溶液的pH<7,其原因为:
NH
4++H
2O

NH
3?H
2O+H
+NH
4++H
2O

NH
3?H
2O+H
+(用离子方程式表示);在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na
+)
小于
小于
c(NO
3-)(选填“大于”、“等于”或“小于”)




 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 随时间变化如图所示.下列说法正确的是
随时间变化如图所示.下列说法正确的是 CH3OH(g)+H2O(g)达到平衡状态的是
CH3OH(g)+H2O(g)达到平衡状态的是
 CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是
CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+ A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题: