
PVB(聚乙烯醇缩丁醛)和PI(聚异戊二烯)均为用途广泛的有机制品,用乙炔为原料制备PVB和PI的流程如图。


(1)A中的官能团名称是 。
(2)已知反应⑤属于加成反应,上述转化中还有 (填序号)也属于该反应类型。
(3)反应③的条件是 。
(4)E是A的同分异构体,E的核磁共振氢谱显示有2种不同化学环境的氢,且E能发生银镜反应E发生银镜反应的化学方程式是 。
(5)反应⑦的化学方程式是 。
(6)依照PI的合成路线,若将反应①中的反应物“ ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是 。
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是 。
(7) ,以
,以 为原料合成
为原料合成 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:2015-2016学年河北省衡水市高一下3月月考化学试卷(解析版) 题型:选择题
核电荷数为1~20的元素中,次外层电子数是最外电子层电子数4倍的元素共有( )
A. 4 种 B. 3 种 C. 2 种 D. l 种
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:实验题
SnSO4是一种重要的硫酸盐,在工业生产中有着广泛的应用。其制备路线如下:
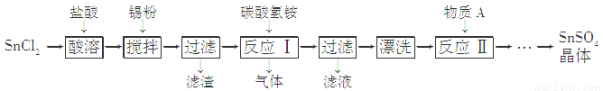
已知:在酸性条件下,溶液中的Sn2+可被空气中的氧气氧化成Sn4+; SnCl2能水解生成碱式氯化亚锡 Sn(OH)Cl]。
(1) 写出物质A的名称:___ _____。
(2) SnCl2用盐酸而不用水溶解的原因是__________ __________(用化学方程式表示)。
(3) 锡粉的作用是除去酸溶时产生的少量Sn4+,请写出产生Sn4+的离子方程式:
_______________ _______________。
(4) 反应Ⅰ生成的沉淀为SnO,写出该反应的化学方程式:_ _ __。该反应的温度需要控制在75 ℃左右的原因是_ _ _ _。
(5) 实验室中“漂洗”沉淀的实验操作方法是_ _ __。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列叙述一定正确的是
A.标准状况下,5.6L SO3含有的分子数为0.25NA
B.标况下,0.1mol苯中含有C=C键数目为0.3NA
C.46g NO2和N2O4的混合气体中含有的原子个数为3NA
D.7.8g过氧化钠与足量CO2反应,转移电子数为0.2NA,CO2为还原剂
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于氧化物的各项叙述正确的是
①酸性氧化物肯定是非金属氧化物
②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物
④金属氧化物都是碱性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥与水反应生成酸的氧化物不一定是酸酐,与水反应生成碱的氧化物不一定是碱性氧化物
⑦不能跟酸反应的氧化物一定能跟碱反应
A.①②③④ B.⑤⑥⑦ C.②③⑥⑦ D.③⑥
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三下学期第五次月考化学试卷(解析版) 题型:选择题
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a
B.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+c(HR-)=c(Na+)
C.将0.2 mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-)
D.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度一定是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三第五次模拟练习化学试卷(解析版) 题型:实验题
NaCl和NaClO在酸性条件下可发生反应:ClO-+ Cl-+2H+ Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出化学反应方程式: 。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分,从而判断该消毒液是否变质。
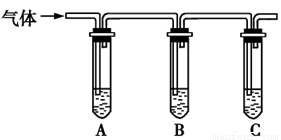
限选试剂:98%浓硫酸、1%品红溶液、1.0 mol·L-1KI-淀粉溶液、1.0 mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
所加试剂 | 预期现象和结论 |
向试管A中加足量①; | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质; |
(3)用滴定法测定消毒液中NaClO的浓度。实验步骤如下:
①量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1Na2SO3溶液b mL。
②滴定分析。将c mol·L-1的酸性KMnO4溶液装入 (填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应。当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据。重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3 NaCl+Na2SO4 ;2KMnO4+5Na2SO3+3H2SO4
NaCl+Na2SO4 ;2KMnO4+5Na2SO3+3H2SO4 K2SO4+2MnSO4+5Na2SO4+3H2O。
K2SO4+2MnSO4+5Na2SO4+3H2O。
③计算。消毒液中NaClO的浓度为 mol·L-1(用含a、b、c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下质检化学试卷(解析版) 题型:选择题
下列物质中,不可能是乙烯的加成产物的是( )
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一下期末化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
A.Z为0.3mol/L B.Y2为0.4mol/L
C.X2为0.2mol/L D.Z为0.4mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com