
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁晶体和金属铜.请根据如下回收流程图,回答有关问题:
(1)加入①为 ,加入②为 (要考虑用量).
(2)操作②的名称为 .
(3)母液中含有的离子有(填离子符号): .
(4)为了得到纯净的FeSO4•7H2O晶体,操作③在蒸发、冷却结晶后还要洗涤FeSO4•7H2O晶体,洗涤FeSO4•7H2O晶体的方法是:
考点: 物质分离和提纯的方法和基本操作综合应用;物质分离、提纯的实验方案设计.
专题: 实验设计题.
分析: 工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,①为Fe,操作①为过滤,C为滤液,且C中含FeSO4,则A中含Cu及过量的Fe,加入②为稀硫酸,操作②为过滤,则B中主要含硫酸亚铁,B、C混合液中主要含FeSO4,操作③为蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,以此来解答.
解答: 解:工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,①为Fe,操作①为过滤,C为滤液,且C中含FeSO4,则A中含Cu及过量的Fe,加入②为稀硫酸,操作②为过滤,则B中主要含硫酸亚铁,B、C混合液中主要含FeSO4,操作③为蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,
(1)由上述分析可知,①为过量Fe,②为适量的硫酸,故答案为:过量Fe;适量的硫酸;
(2)由上述分析可知,操作②分离不溶性固体与溶液,则为过滤,故答案为:过滤;
(3)由B、C混合液中主要含FeSO4,可知蒸发、浓缩、结晶、过滤母液中含有的离子有Fe2+、SO42﹣,故答案为:Fe2+、SO42﹣;
(4)洗涤FeSO4•7H2O晶体的方法是将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可,故答案为:将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可.
点评: 本题考查混合物分离提纯的综合应用,为高频考点,把握物质的性质、发生的反应及除杂的原则等为解答的关键,侧重分析、实验能力的考查,注意实验技能的应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列实验处理不可行的是( )
①将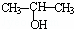 与NaOH的醇溶液共热制备CH3﹣CH═CH2
与NaOH的醇溶液共热制备CH3﹣CH═CH2
②向甲酸(H﹣COOH)和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热,检验混合物中是否含有甲醛
③向丙烯醛(CH2=CH﹣CHO)中滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
④为验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再滴入几滴硝酸银溶液,观察现象.
|
| A. | 只有①③ | B. | 只有①②④ | C. | 只有②③④ | D. | 都不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
配制物质的量浓度的溶液,造成浓度偏高的操作是()
A. 定容时,滴加蒸馏水超过刻度线
B. 定容时,眼睛俯视刻度线
C. 洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D. 定容时,眼睛仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氧化物能否与酸或碱反应生成盐和水的性质,可把氧化物分为碱性氧化物、酸性氧化物、两性氧化物和不成盐氧化物,这种分类方法称为 分类法(填“交叉”或“树状”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关CuSO4溶液的叙述正确的是( )
A. 该溶液中Na+、NH4+、NO3﹣、Mg2+可以大量共存
B. 通入CO2气体产生蓝色沉淀
C. 与H2S反应的离子方程式:Cu2++S2﹣=CuS↓
D. 与过量浓氨水反应的离子方程式:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
在无色酸性溶液中能大量共存的离子组是( )
A. NH4+、Fe3+、SO42﹣、Cl﹣ B. Ba2+、K+、OH﹣、NO3﹣
C. Al3+、Cu2+、SO42﹣、Cl﹣ D. Na+、Ca2+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液含有Na+、Ba2+、Cu2+、HCO3﹣、SO42﹣、Cl﹣等离子中的若干种.依次进行下列实验,现象如下:
①取少量溶液于试管之中,滴入几滴紫色石蕊试液后溶液显红色;
②另取少量的原溶液,先加入过量的NaOH溶液,然后再滴加适量的Na2CO3溶液,产生白色沉淀.
请回答下列问题:
(1)原溶液中肯定存在的离子有 ;
原溶液中肯定不存在的阳离子有 ,
(3)写出②中发生反应的离子方程式: ; .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. 使甲基橙变红色的溶液:Mg2+、K+、SO42﹣、NO3﹣
B. 使酚酞变红色的溶液:Na+、Cu2+、HCO3﹣、NO3﹣
C. 0.1 mol•L﹣1AgNO3溶液:H+、K+、SO42﹣、I﹣
D. 0.1 mol•L﹣1NaAlO2溶液:H+、Na+、Cl﹣、SO42﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com