
【题目】下列解释物质用途或现象的反应方程式不准确的是( )
A.硫酸型酸雨的形成会涉及反应:2H2SO3+O2 ![]() 2H2SO4
2H2SO4
B.工业上制取粗硅的化学方程式:SiO2+C ![]() Si+CO2↑
Si+CO2↑
C.Na2 S2O3溶液中加入稀硫酸:S2O+2H ![]() ═SO2+S↓+HO2
═SO2+S↓+HO2
D.成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
【答案】B
【解析】A.正常雨水溶解二氧化碳,酸雨中溶解二氧化硫,酸性增强,二氧化硫与水反应生成H2SO3,H2SO3可被氧化生成H2SO4,则硫酸型酸雨的形成会涉及反应为:2H2SO3+O2 ![]() 2H2SO4,故A不符合题意;
2H2SO4,故A不符合题意;
B.工业上制硅的反应方程式为:SiO2+2C ![]() Si+2CO↑,故B符合题意;
Si+2CO↑,故B符合题意;
C.Na2S2O3溶液中加入稀硫酸发生氧化还原反应,生成S、二氧化硫、水,该反应为Na2S2O3+H2SO4═Na2SO4+SO2+S↓+H2O,该离子反应为S2O32﹣+2H+=S↓+SO2↑+H2O,故C不符合题意;
D.盐酸与次氯酸钠反应生成氯气,反应的离子方程式为Cl﹣+ClO﹣+2H+=Cl2↑+H2O,故D不符合题意;
故答案为:B.
A.亚硫酸被氧化为硫酸;
B.碳还原二氧化硅生成硅和一氧化碳;
C.硫代硫酸钠与稀硫酸反应生成二氧化硫、单质硫和水;
D.盐酸与次氯酸钠中不同价态的氯元素发生氧化还原反应生成氯气.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于氯水的说法正确的是( )
A. 新制氯水中只含Cl2和H2O分子
B. 光照氯水有气泡冒出,该气体是氯气
C. 新制氯水可使蓝色石蕊试纸先变红后褪色
D. 氯水放置数天后pH将变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《神农本草经》记载,神农尝百草,日遇七十二毒,得茶而解。茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
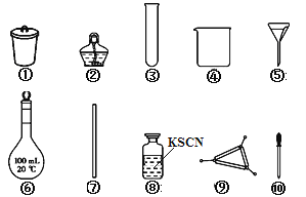
A. 将茶叶灼烧灰化,选用①、②和⑨
B. 用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C. 过滤得到滤液,选用④、⑤和⑦
D. 检验滤液中的Fe3+,选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定乙醇的结构式,有人设计了用无水酒精与钠反应的实验装置和测定氢气体积的装置进行实验.可供选用的实验仪器如图所示: 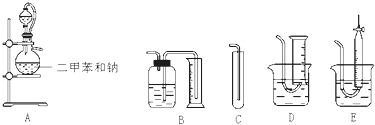
请回答以下问题:
(1)测量氢气体积的正确装置是(填写编号).
(2)装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是(填写编号).
A.防止无水酒精挥发
B.保证实验装置不漏气
C.使无水酒精容易滴下
(3)实验前预先将一小块钠在二甲苯中熔化成若干个小钠珠,冷却后倒入烧瓶中,其目的是 .
(4)已知无水酒精的密度为0.789gcm﹣3 , 移取2.0mL酒精,反应完全后(钠过量),收集到390mL(视作标准状况)气体.则一个乙醇分子中能被钠取代出的氢原子数为 , 由此可确定乙醇的结构简式为而不是 .
(5)实验所测定的结果偏高,可能引起的原因是(填写编号).
A.本实验在室温下进行
B.无水酒精中混有微量甲醇
C.无水酒精与钠的反应不够完全.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )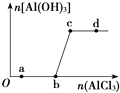
A.a点对应的溶液中:Na+、Fe3+、SO42﹣、HCO3﹣
B.b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
C.c点对应的溶液中:Ag+、Ca2+、NO3﹣、F﹣
D.d点对应的溶液中:K+、NH4+、I﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是
( )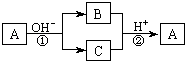
A.X元素可能为Al
B.X元素一定为非金属元素
C.反应①和②互为可逆反应
D.反应①和②不可能都为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于实验室制备乙烯的实验,下列说法正确的是( )
A.反应物是乙醇和过量的3摩/升硫酸的混和液
B.温度计插入反应溶液液面以下,以便控制温度在140℃
C.反应容器(烧瓶)中应加入少许瓷片
D.反应完毕先灭火再从水中取出导管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H22NH3 . 已知加入1molN2和4molH2时,达到平衡后生成amolNH3 . 有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
已知 | 起始状态物质的量/mol | 平衡时NH3的 | ||
N2 | H2 | NH3 | ||
1 | 4 | 0 | a | |
① | 1.5 | 9 | 0 | |
② | 1 | 0.5a | ||
③ | m | g(g≥4m) | 0 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com