
【题目】下列转化过程中,氮元素化合价升高的是( )
A.雷雨条件下大气中的N2转变为HNO3
B.高温高压和Fe催化条件下工业合成NH3
C.蓝藻等原核生物将N2转变为铵盐
D.化肥NH4HCO3在使用中分解为NH3
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺如图所示:

(1)对青蒿干燥破碎后,加入乙醚的目的是______。
(2)操作Ⅰ需要的玻璃仪器主要有烧杯、______,操作Ⅱ的名称是______。
(3)操作Ⅲ的主要过程可能是______(填字母)。
A. 加水溶解,蒸发浓缩、冷却结晶B. 加95%的乙醇,浓缩、结晶、过滤C. 加入乙醚进行萃取分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中不能用勒夏特列原理解释是
A. 由H2、I2(g)、HI(g)气体组成的平衡体系压缩体积后颜色变深
B. 实验室常用排饱和食盐水法收集氯气
C. 红棕色的NO2,加压后颜色先变深后变浅
D. 工业制取金属钾[Na(l)+KCl(l)![]() NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来
NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”月光穿过薄雾形成的种种美景的本质原因是
A. 光是一种胶体 B. 雾是一种胶体
C. 发生丁达尔效应 D. 空气中的小水滴颗粒直径大小约为1nm~100nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态Cl原子中,电子占据的最高能层具有的原子轨道数为____。
(2)NH4CuSO3中金属阳离子的价电子排布式为________。N、O、S三种元素的第一电离能由大到小的顺序为________ (填元素符号)。
(3)氨基乙酸钠(H2NCH2COONa)中中心原子N原子的价层电子对数为________,C原子的杂化方式为________,1 mol氨基乙酸钠中含有σ键的数目为________。
(4)向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4溶液,在[Cu(NH3)4]2+中配原子为________。
(5)MgO和CaO均为离子晶体,两者的熔融混合物冷却时,先析出的晶体是____,原因是________
(6)BN的熔点是3000℃,密度为d g·cm-3,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有________个;若原子半径分别为rN pm和rB pm,阿伏加德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为__________(用含d、rN 、rB、NA的式子表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组用镍触媒废料(主要成分为Ni-Al合金,混有少量Fe、Cu、Zn及有机物) 制备NiO并回收金属资源的流程如下所示:
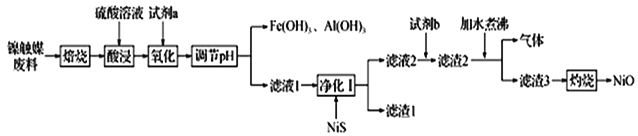
已知:相关数据如表1和表2所示
表1部分难溶电解质的溶度积常数(25℃)
物质 | Ksp | 物质 | Ksp |
Fe(OH)3 | 4.0×10-38 | CuS | 6.3×10-34 |
Fe(OH)2 | 1.8×10-16 | ZnS | 1.6×10-24 |
Al(OH)3 | 1.0×10-33 | NiS | 3.2×10-18 |
Ni(OH)2 | 2.0×10-15 |
表2 原料价格表
物质 | 价格/(元吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
请回答下列问题:
(1)“焙烧”的目的是________________________________。
(2)“试剂a”的名称为__________________;选择该试剂的理由是______。
(3)“氧化”时反应的离子方程式为__________________________________________。
(4)欲使溶液中Fe3+和A13+的浓度均小于等于1.0×10-6 mol L-1,需“调节pH”至少为_______________。
(5)“试剂b”应选择__________,“加水煮沸”时,反应的化学方程式为_______________________________。
(6)氢镍电池是一种应用广泛的二次电池,放电时,该电池的总反应为NiOOH+MH=Ni(OH)2+M,当导线中流过2 mol电子时,理论上负极质量减少__________g。充电时的阳极反应式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁和水反应放出大量热,该反应可用于野外供热。下列镁和水反应放热最快的是( )
A.100g镁条和100mL冰水反应
B.100g镁粉和100mL30℃水反应
C.100g镁条和100mlL30℃水反应
D.100g镁粉和100mL冰水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH)
B、C60和石墨
C、![]() 和
和![]()
D、35Cl和37Cl
E、乙醇和乙二醇
①互为同位素的是______________;
②互为同系物的是_________________;
③互为同素异形体的是__________;
④互为同分异构体的是_____________;
(2)梯恩梯(TNT)结构简式为____________________________;
(3)某有机聚合物物结构为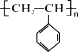 ,试回答下列问题:
,试回答下列问题:
①有机物名称是___________________,链节为______。
②实验测得该高聚物的相对分子质量(平均值)为52000,则该高聚物的聚合度n为________。
(4)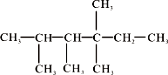
①有机物名称是__________________________。
②此有机物为烯烃加成的产物,则原来烯烃的结构可能有_______种。
(5)某物质结构如图所示,分子式为_________________;该物质可以与下列_____(填序号)发生反应。
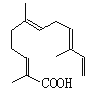
A.酸性KMnO4溶液 B.氢气
C.溴水 D.NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com