
��10�֣���������������ˮ��ɱ��������
��1����ҵ�������缫��ʯī��Ϊ�缫��ⱥ��ʳ��ˮ����������ʯī�缫�ϵĵ缫��ӦʽΪ_____________
������������һ�������£���Cl2����ˮ�е�CN������������N2��CO2���÷�Ӧ�����ӷ���ʽΪ_________
��2���Ȱ���NH2Cl��������������Һ�ȴ�������ˮ��ͬʱͨ������������������Ӧ��Cl2+NH3�TNH2Cl+HCl�����ɵ�NH2Cl��HClO�ȶ������ܲ���ˮ����������HClO��������ɱ�������ã�
�Ȱ�������ɱ����ԭ���� ���û�ѧ����ʽ��ʾ����
��3����ˮ����ֳ�У�������Na2S2O3��ˮ�в������Cl2��ȥ��ijʵ��С��������ͼ1��ʾװ�ú�ҩƷ�Ʊ�Na2S2O3��
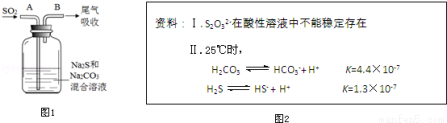
����������ϻش�
�ٿ�ʼͨSO2ʱ����B�ڼ����µ��������ɣ��жϴ�B���ų����������Ƿ���H2S����д���ж�����__________________________��
��Ϊ��ý϶��Na2S2O3������Һ��pH�ӽ�7ʱ��Ӧ����ֹͣͨ��SO2����ԭ���� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�߰��и�����ѧ�ڵڶ��ζο���ѧ�Ծ��������棩 ���ͣ������
��������(SeO2)��һ�����������䱻��ԭ��ĵ��������ܳ�Ϊ������Ⱦ�ͨ����ŨHNO3��ŨH2SO4��Ӧ����SeO2�Ի���Se�����������գ�
��1��Se��ŨHNO3��Ӧ�Ļ�ԭ����ΪNO��NO2����NO��NO2�����ʵ���֮��Ϊ1��1��д��Se��ŨHNO3�ķ�Ӧ����ʽ___ _____��
��2����֪��Se + 2H2SO4(Ũ) �� 2SO2�� + SeO2 + 2H2O
2SO2 + SeO2 + 2H2O �� Se + 2SO42�� + 4H+
SeO2��H2SO4(Ũ)��SO2����������ǿ������˳����_____________________��
��3�����յõ���SeO2�ĺ���������ͨ������ķ����ⶨ��
�� SeO2 + KI + HNO3 �� Se + I2 + KNO3 + H2O �� I2 + 2Na2S2O3 �� Na2S4O6 + 2NaI
��ƽ����ʽ�٣��������ת�Ƶķ������Ŀ________________________________��
��4��ʵ���У�ȷ����SeO2��Ʒ0.1500 g��������0.2000 mol/L��Na2S2O3��Һ25.00 mL�����ⶨ����Ʒ��SeO2����������Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡӢ���и�����ѧ�ڵڶ����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������������
A���������������������ռ�����ᷴӦ����������������ͬ
B���Ʊ���������ʱ���ñ��͵�NaO H��Һ�ռ������Գ�ȥ���е�����
H��Һ�ռ������Գ�ȥ���е�����
C���ñ���ʳ��ˮ���ˮ����ʯ��Ӧ�����Լ�����Ȳ�IJ�������
D��SO2ʹ��ˮ��ɫ����ϩʹKMnO4��Һ��ɫ��ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������и�����ѧ�����в������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ���������ճ�������������Ҫ��Ӧ�á�����˵������ȷ����
A�������ѧ�Ҹ����ڹ��˴�����Ϣ������ȡ��ͻ���Գɾͣ����˵���Ҫ�ɷ��Ǹߴ��ȵĶ�������
B�����͡�Ư�ۡ�ˮ��������ˮ��Ϊ�����
C�����������������ȼú����������β����������������߿�������
D����װʳƷ�ﳣ�й轺��ʯ�ҡ���ԭ��������С������������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ�ڵ�һ����ϲ��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ�ϳɰ����Ʊ�HNO3һ����������������������£�
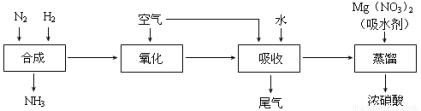
��д����ҵ�ϳɰ��Ļ�ѧ����ʽ ������β���е�NO2һ�������¿��백����Ӧת��Ϊ��������÷�Ӧ�Ļ�ѧ����ʽΪ ��
��ijͬѧ��ʵ����������Mg(NO3)2��ϡ������ȡŨ���ᣬ�����ܡ��ƾ��ơ�ţ�ǹܡ���ƿ�⣬����IJ��������� ��
��2��ij��ȤС�������ͼװ����ȡ��̽��SO2��������ʡ�
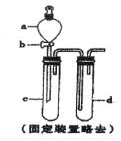
������ʵ�鷽����������ͼ��ʾװ����ȡ����SO2����_________������ţ�
A.Na2SO3��Һ��HNO3 B.Na2SO3������Ũ����
C.�������ڴ�����ȼ�� D.ͭ��ŨH2SO4
����װ���������װ�������Եķ����ǣ�________
����Ҫ֤��c�����ɵ�������SO2��d�м���Ʒ����Һ����b����Ӧ��ʼ����d����Һ_____________����________________����ʵ��IJ������Թ�d�е���Һ����ɫ�ָֻ���֤��������SO2��
��ָ����ʦָ��Ӧ����һβ������װ�ã�������ͬѧ�����������װ�ã����к�������______________������ţ���
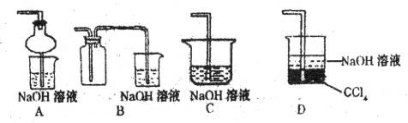
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ�°���У��������ѧ�ڵڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
ijʵ�������ͼ��ʾ,��ͼ���Թ��е�������

A��ͭƬ�ܽ�,������ɫ����,��������������Ϊ����ɫ
B��ͭƬ�ܽ�,������ɫ����,������������������ɫ
C��ͭƬ�ܽ�,�ų�����ɫ�д̼�����ζ������
D������������,��ϡ�����ͭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶���ѧ�����б���ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ�ϳ����ú����ˮ��������Na2S2O3��5H2O��ʵ���ҿ�������װ��(��ȥ���ּг�����)ģ���������̡�
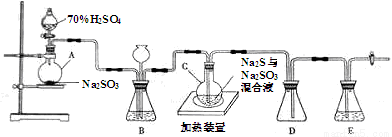
��ƿC�з�����Ӧ���£�
Na2S��H2O��SO2��Na2SO3��H2S (��)
2H2S��SO2��3S��2H2O (��)
S��Na2SO3��Na2S2O3 (��)
��1��������װ��ɺر����˻�������װ��B�еij���©����ע��Һ�����γ�һ��Һ������ ��������װ�����������á�װ��D�������� ��װ��E��Ϊ ��Һ��
��2��Ϊ��߲�Ʒ���ȣ�Ӧʹ��ƿC��Na2S��Na2SO3ǡ����ȫ��Ӧ������ƿC��Na2S��Na2SO3���ʵ���֮��Ϊ ��
��3��װ��B������֮һ�ǹ۲�SO2���������ʣ����е�Һ�����ѡ�� ��
a������ˮ b������Na2SO3��Һ
c������NaHSO3��Һ d������NaOH��Һ
��4����Ӧ��ֹ����ƿC�е���Һ������Ũ����������Na2S2O3��5H2O�����п��ܺ���Na2SO3��Na2SO4�����ʡ����������Լ���ϡ���ᡢϡ���ᡢϡ���ᡢBaCl2��Һ��AgNO3��Һ�����ʵ�飬����Ʒ���Ƿ����Na2SO4����Ҫ˵��ʵ�����������ͽ��ۣ� ��
��֪Na2S2O3��5H2O�����ֽ⣺S2O32-��2H+��S����SO2����H2O
��5��Ϊ�˲ⶨij������Ʒ�ijɷ֣���ȡ����������ͬ�ĸ���Ʒ���ֱ������ͬŨ�ȵ�������Һ20mL����ַ�Ӧ���˳�������Һʹ���ɵ�SO2ȫ���ݳ���
����й�ʵ���������£���״������
��һ�� | �ڶ��� | ������ | |
��Ʒ������/g | 12.60 | 18.90 | 28.00 |
������������/L | 1.12 | 1.68 | 2.24 |
����������Һ�����ʵ����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��Զ�и߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�������ȷ�Ӧ����
A��C6H12O6�������ǣ�+6O2 6CO2+6H2O
6CO2+6H2O
B��CH3COOK+H2O  CH3COOH+KOH
CH3COOH+KOH
C��A+B C+D�� ��H<0
C+D�� ��H<0
D���ƻ�������ȫ����ѧ����������С���ƻ���Ӧ��ȫ����ѧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡӢ��ѧУ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ȡ�����ͬ������ͬ��ͬѹ�£��ֱ����CO���������ֻ�����壬���������ȵ�״������ͼ��ʾ��A��B��C��D�ĸ������ڣ���CO����ԭ����һ����ȵ���
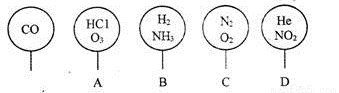
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com