硫元素具有可变价态,据此完成以下有关含硫化合物性质的试题.
(1)将H
2S气体通入FeCl
3溶液中,现象是
;反应的离子方程式是
.
(2)为了探究-2价硫的化合物与+4价硫的化合物反应的条件,设计了下列实验.
|
实验操作 |
实验现象 |
| 实验1 |
将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 |
无明显现象 |
| 实验2 |
将H2S通入Na2SO3溶液中 |
未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 |
将SO2通入Na2S溶液中 |
有浅黄色沉淀产生 |
已知:电离平衡常数:H
2S K
1=1.3×10
-7;K
2=7.1×10
-15 H
2SO
3 K
1=1.7×10
-2;K
2=5.6×10
-8①根据上述实验,可以得出结论:在
条件下,+4价硫的化合物可以氧化-2价硫的化合物.
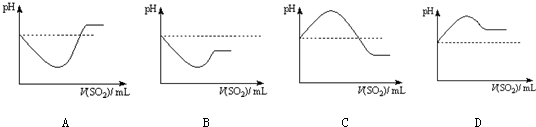
②将SO
2气体通入H
2S水溶液中直至过量,下列表示溶液pH随SO
2气体体积变化关系示意图正确的是
(选填编号).
(3)现有试剂:溴水、硫化钠溶液、Na
2SO
3溶液、稀硫酸、NaOH溶液、氨水.要证明Na
2SO
3具有还原性,应选用的试剂有
,看到的现象是
.要证明Na
2SO
3具有氧化性,应选用的试剂有
,反应的离子方程式是
.
(4)文献记载,常温下H
2S可与Ag发生置换反应生成H
2.现将H
2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H
2S与Ag发生了置换反应
.




 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案