
200ml 0.2mol/L 的NaOH溶液与300ml 0.1mol/L 的稀硫酸混合,混合后Na+的物质的量浓度是 ( )
A.0.2mol/L B.0.06 mol/L C.0.12 mol/L D.0.08mol/L
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:选择题
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
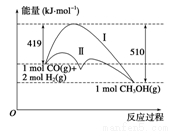
A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高二9月月考化学卷(解析版) 题型:选择题
合成氨反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是

A.t1时升高了温度 B.t2时使用了催化剂 C.t3时增大了压强 D.t4时降低了温 度
度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷(解析版) 题型:选择题
关于0.1 mol·L-1 Na2CO3溶液的叙述错误的是
A.0.5 L该溶液中钠离子的物质的量浓度为0.2 mol·L-1
B.1 L该溶液 中含Na2CO3的质量为10.6 g
中含Na2CO3的质量为10.6 g
C.从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.01 mol·L-1
D .取该溶液10 mL,加水稀释至100 mL后,Na2CO 3的物质的量浓度为0.01 mol·L-1
3的物质的量浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是( )
A.500mL溶液中Cl-离子浓度为0.2mol·L-1
B.500mL溶液中Ba2+离子浓度为0.2mol·L-1
C.500mL溶液中Cl-离子总数为0.2NA
D.500mL溶液中Ba2+和Cl-离子总数为0.3NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高二9月月考化学卷(解析版) 题型:选择题
55g铁铝混合物与足量的盐酸反应生成标准状况下的氢气44.8L,则混合物中铁和铝的物质的量之比为
A.1:1 B.1:2 C.2:1 D.2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高二9月月考化学卷(解析版) 题型:选择题
甲、乙、丙、丁分别是BaCl2 、NaOH、FeCl2、Al2(SO4)3、四种物质中的一种。若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生。据此可推断丙物质是
A.BaCl2 B.NaOH C.FeCl2 D.Al2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上9.18周考化学卷(解析版) 题型:实验题
根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
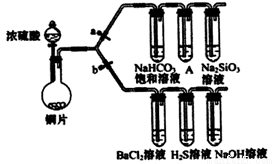
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、__________、加药品后,打开。关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_____________,装置A中的试剂是____________。
③ 能说明碳的非金属性比硅强的实验现象是:_________________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 打开b,关闭a。能验证SO2具有氧化性的化学方程式是:______________。
② 若大量的SO2通入NaOH溶液中,其化学方程式是:_______________。
③ BaCl2溶液中无沉淀现象,将其分成两份,分滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
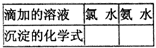
写出其中SO2显示还原性并生成沉淀的离子方程式_____________。
查看答案和解析>>
科目:高中化学 来源:2017届天津一中高三上第一次月考化学试卷(解析版) 题型:实验题
(一)某化学研究性学习小组讨论Fe3+和SO32﹣之间发生怎样的反应,提出了两种可能;一是发生氧化还原反应:2Fe3++SO32﹣+H2O=2Fe2++SO42﹣+2H+;二是发生双水解反应:2Fe3++3SO32﹣+6H2O=2Fe2++2Fe(OH)3(胶体)+3H2SO4,为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
实验Ⅰ:学生选择的实验用品:N a2SO3浓溶液,BaCl2稀溶液,稀盐酸,试管若干,胶头滴管若干,从选择的药品分析,设计这个实验的目的是 .
a2SO3浓溶液,BaCl2稀溶液,稀盐酸,试管若干,胶头滴管若干,从选择的药品分析,设计这个实验的目的是 .
实验Ⅱ:取5mL FeCl3浓溶液于试管中,再滴加入 Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色,这种红褐色液体是 向红褐色液体中加入稀盐酸至过量,将所得溶液分为两等份,其中一份加入KSCN溶液变成血红色,反应的离子方程式为 .另一份加入BaCl2稀溶液有少量白色沉淀生成,产生该白色沉淀的离子方程式是 .
实验Ⅲ:换成两种稀溶液重复实验Ⅱ,产生现象完全相同,由上述实验得出的结论是
若在FeCl3溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无 色气体,该反应的化学方程式是 .
色气体,该反应的化学方程式是 .
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看出,二者的水溶液与FeCl3溶液反应现象差别很大,分析其可能的原因是:① ;② .
(二)镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:

①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为__________。
②滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com