

| A.该反应的还原剂是Cl— |
| B.消耗1 mol还原剂,转移6 mol电子 |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.反应后溶液的酸性明显增强 |
科目:高中化学 来源:不详 题型:单选题
| A.②①④③ | B.①②③④ | C.②④①③ | D.①③④② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
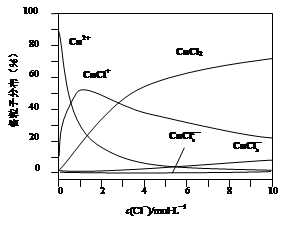
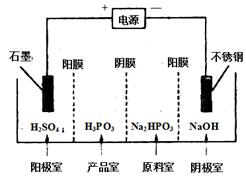
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O2既是氧化剂,又是还原剂 |
| B.Fe2O3在反应中得到电子 |
| C.3 mol Na2O2参加反应,转移的电子总数为12mol |
| D.Na2FeO4能消毒杀菌,因其具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1?:4 | B.1?:2 |
| C.2?:1 | D.4?:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.8 mol | B.1.1 mol | C.1.2 mol | D.2.0 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应过程中,电子转移数为2NA |
| B.固体生成物的质量为106 g |
| C.CO可能有剩余 |
| D.反应后一定生成11.2 L氧气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8.64 g | B.9.20 g |
| C.9.00 g | D.9.44 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com