
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 16种 |
分析 分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,根据羧酸与醇组合,计算同分异构体数目即可.
解答 解:分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,属于饱和一元酯,若为甲酸和丁醇酯化,丁醇有4种;
若为乙酸和丙醇酯化,丙醇有2种;
若为丙酸和乙醇酯化,丙酸有1种;
若为丁酸和甲醇酯化,丁酸有2种;
故羧酸共有5种,醇共有8种,其中相同碳原子数的酸与醇分别为:甲酸与甲醇、乙酸与乙醇、丙酸与丙醇(有2种:正丙醇与异丙醇)、丁酸(有2种)与丁醇(丁醇有4种),故总共有:1+1+2+2×4=12种,
故选C.
点评 本题考查酯类的水解规律,同分异构体的书写与判断,难度较大,掌握丙基有2种、丁基有4种结构是解决本题的关键.


科目:高中化学 来源: 题型:解答题
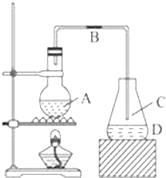 某化学课外小组用如图装置制取溴苯,请按要求完成下列小题:
某化学课外小组用如图装置制取溴苯,请按要求完成下列小题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测①中现象 |
| A | 酚酞溶液 | 浓氨水 | 无色变红色 |
| B | 湿润红布条 | 饱和氯水 | 红布条褪色 |
| C | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| D | 硝酸银溶液 | 浓盐酸 | 有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有七个主族,八个副族 | |
| B. | IA族的元素全部是金属元素 | |
| C. | 元素周期表的第三列(从左往右)所含元素种类最多 | |
| D. | 元素周期表有三个长周期(均含18种元素),三个短周期(均含8种元素) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
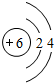
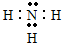
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
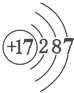
| A. | X属于金属元素 | B. | 该原子的核外电子数为7 | ||
| C. | X与Na形成的化合物为NaX | D. | 该原子最外电子层达到了稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y>Z>X | B. | Z>X>Y | C. | X>Y>Z | D. | Y>X>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
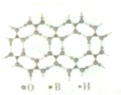 元素周期表可以指导我们寻找和合成成新的物质,如金属和非金属分界线附近的元素可用于制造半导体材料,是科学研究的热点
元素周期表可以指导我们寻找和合成成新的物质,如金属和非金属分界线附近的元素可用于制造半导体材料,是科学研究的热点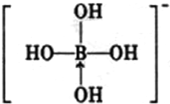 或
或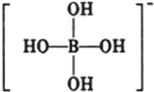 ,硼酸具有层状结构,每层结构如图所示,每摩尔晶体中所含氢键的数目为3NA(设NA为阿伏伽德罗常数的值)
,硼酸具有层状结构,每层结构如图所示,每摩尔晶体中所含氢键的数目为3NA(设NA为阿伏伽德罗常数的值)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
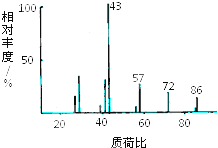 某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则:
某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com