
下列有关物质的性质与应用均正确的是
A.MgO的熔点很高,可用于制作耐高温材料
B.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C.氨气是一种碱性气体,可用P2O5或无水CaCl2干燥
D.SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力
科目:高中化学 来源:2016届广西省钦州市钦南区高三上学期期中质量调研测试化学试卷(解析版) 题型:选择题
Zn(OH)2是两性氢氧化物,和强酸反应时生成Zn2+,跟强碱反应时生成ZnO22-.现有三份等物质的量浓度、等体积的MgCl2、ZnCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如下图所示,则与MgCl2、ZnCl2、AlCl3三种溶液一一对应的正确图象是

A.③②① B.③②④ C.③⑤① D.③⑤④
查看答案和解析>>
科目:高中化学 来源:2016届湖北省松滋市高三上学期期中测试化学试卷(解析版) 题型:选择题
X、Y均为元素周期表ⅦA族中的两种元素。下列叙述中,能够说明X的原子得电子能力比Y强的是
A.原子的电子层数:X>Y
B.对应的简单离子的还原性:X>Y
C.气态氢化物的稳定性:X>Y
D.氧化物对应水化物的酸性:X>Y
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南通市高三上学期第一次阶段测化学试卷(解析版) 题型:实验题
硼镁矿属于硼酸盐,可用来制备硼酸(H3BO3)和MgO,方法如下:硼镁矿粉与(NH4)2SO4溶液混合后加热,反应生成H3BO3晶体和MgSO4溶液,同时放出NH3;再向MgSO4溶液中通入NH3与CO2,得到MgCO3沉淀和滤液,沉淀经洗涤、煅烧后得MgO,滤液则循环使用。回答下列问题:
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式 。
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是 。
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式 。
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南通市高三上学期第一次阶段测化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动
B.铅蓄电池在放电过程中,负极质量增加,正极质量减少
C.100 mL pH=3的HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA酸性比HB弱
D.已知
 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
查看答案和解析>>
科目:高中化学 来源:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷(解析版) 题型:填空题
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯。
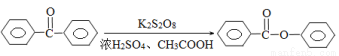
制备苯甲酸苯酯的实验步骤为:
步骤1:将20mL浓H2SO4与40mL冰醋酸在下图装置的烧杯中控制在5℃以下混合。

步骤2:向烧杯中继续加入过硫酸钾25g,用电磁搅拌器搅拌4~5分钟,将二苯甲酮9.1g溶于三氯甲烷后,加到上述混合液中,控制温度不超过15℃,此时液体呈黄色。
步骤3:向黄色液体中加水,直至液体黄色消失,但加水量一般不超过1mL,室温搅拌5h。
步骤4:将反应后的混合液倒入冰水中,析出苯甲酸苯酯,抽滤产品,用无水乙醇洗涤,干燥
(1)步骤1中控制在5℃以下混合的原因为 。
(2)步骤2中为控制温度不超过15℃,向混合液中加入二苯甲酮的三氯甲烷溶液的方法是 。
(3)步骤3中加水不超过1mL,原因是 。
(4)步骤4中抽滤用到的漏斗名称为 。
(5)整个制备过程中液体混合物会出现褐色固体,原因是 ;除去该固体操作为 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷(解析版) 题型:选择题
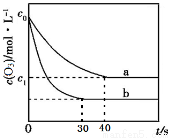
臭氧的脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),一定条件下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是
N2O5(g)+O2(g),一定条件下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是
A.反应2NO2(g)+O3(g) N2O5(g)+O2(g) △S<0
N2O5(g)+O2(g) △S<0
B.曲线b对应的条件改变可能是加入了催化剂,平衡常数Ka=Kb
C.曲线b对应的条件改变可能是密闭容器的体积变为4.0 L
D.若c1=0.3mol·L-1,从反应开始到平衡时该反应的速率v(NO2)=0.005 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:填空题
实验题:现需要90 mL 1.00 mol·L-1 NaCl溶液,某同学按下列步骤进行配制:
①计算所需NaCl固体的质量;
②称量NaCl固体;
③将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解;
④将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶;
⑤向容量瓶中加蒸馏水至刻度线。
请回答有关问题:
(1)计算所需NaCl固体的质量______g。
(2)为了加速溶解,可以采取的措施是_______________。
(3)使用容量瓶的规格是________mL。
(4)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求______________(填“大”或“小”)了。
(5)如果某同学是用托盘天平称量NaCl固体,那么称量的质量是 ,与计算量一致吗?解释原因___________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州地区七校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列物质既能由金属和酸反应获得,也能通过金属和氯气反应获得的是
A. CuCl2 B. FeCl2 C. FeCl3 D. NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com