
 .
.分析 根据Y与氧气反应生成水和单质Z,Y+O2→Z(无色、无味的气体)+H2O,Z为无色、无味气体,可确定组成Z的元素为氮,则Y是NH3;根据反应①W+H2O→X(白色沉淀)+Y(无色、具有刺激性气味的气体),利用元素守恒,可以确定5种物质共涉及4种元素,其中3种为氢、氧、氮,根据原子序数之和等于28,可以确定另一种元素为镁.则可推出X为Mg(OH)2、V为MgO、W为Mg3N2,
(1)依据分析可知X为MgO V为Mg3N2 W为Mg(OH)2;
(2)Y为NH3属于共价化合物,氮原子和三个氢原子形成三对共用电子对;
(3)反应①是氮化镁和水反应生成氨气和氢氧化镁沉淀;
②的反应为氢氧化镁受热分解生成氧化镁和水.
解答 解:根据Y与氧气反应生成水和单质Z,Y+O2→Z(无色、无味的气体)+H2O,Z为无色、无味气体,可确定组成Z的元素为氮,则Y是NH3;根据反应①W+H2O→X(白色沉淀)+Y(无色、具有刺激性气味的气体),利用元素守恒,可以确定5种物质共涉及4种元素,其中3种为氢、氧、氮,根据原子序数之和等于28,可以确定另一种元素为镁.则可推出X为Mg(OH)2、V为MgO、W为Mg3N2,
(1)依据分析可知X为MgO V为Mg3N2 W为Mg(OH)2,故答案为:MgO,Mg3N2,Mg(OH)2 ;
(2)氨气为共价化合物,氨气中存在3个氮氢键,氮原子最外层达到8电子稳定结构,氨气的电子式为 ,故答案为:
,故答案为: ;
;
(3)反应①是氮化镁和水反应生成氨气和氢氧化镁沉淀,反应的化学方程式为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑,
②的反应为氢氧化镁受热分解生成氧化镁和水,反应的化学方程式为:Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O,
故答案为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
点评 本题考查了物质转化关系分析,物质性质的理解应用,主要是氮及其化合物性质的熟练掌握,题目难度中等.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的溶液中:Na+、K+、MnO4-、NO3- | |
| B. | pH=13的溶液中:Na+、K+、SO42-、HCO3- | |
| C. | 0.1mol•L-1NaClO溶液中:Na+、K+、I-、NO3- | |
| D. | 0.1mol•L-1FeCl3溶液中:NH4+、SCN-、Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
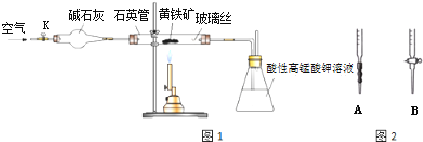
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,在选择萃取剂时,要求萃取剂和原溶剂不互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲装置为铁的析氢腐蚀,若将铁换成铜,则甲装置就是铜的吸氧腐蚀 | |
| B. | 若将甲装置中的电流表改为电源,无论电源怎么连接,C电极上都会有气体放出 | |
| C. | 乙装置中K关闭后,a极附近颜色逐渐加深变黑 | |
| D. | 若将乙装置中的NaOH溶液换为HCl溶液,则K关闭后b极颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验目的 | 实验操作 | |
| A | 鉴别Al3+和Fe3+ | 分别加入少量NaOH溶液 |
| B | 比较Fe和Cu的金属活动性 | 分别加入浓硝酸 |
| C | 证明品红溶液褪色的原因是通入了SO2 | 将褪色后的溶液再加热 |
| D | 分离乙酸乙酯和乙酸 | 加饱和NaOH溶液,蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
| ② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com