
 Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题:
Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题: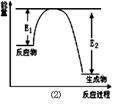

 (正)
(正)  (逆)。
(逆)。
 (正) >
(正) >  (逆)③ 1mol/(L·min);④ 75% ;
(逆)③ 1mol/(L·min);④ 75% ; Si3N4 + 6CO中C的化合价由0价→+2价,作还原剂,N元素的化合价由反应前的N2的0价→-3价,得到电子,作氧化剂,变为还原产物Si3N4。(2)由于反应物的能量比生成物的能量高,多余的能量释放出来。所以该反应是放热反应。(3)①由图像可知M是生成物,N的反应物。在反应方程式中,反应物中只有N2是气体,生成物中只有CO是气体,因此M是CO ,N是N2。②在t2时刻,CO 和N2的物质的量浓度相等,由于反应还没有达到平衡,此时正逆反应速率大小
Si3N4 + 6CO中C的化合价由0价→+2价,作还原剂,N元素的化合价由反应前的N2的0价→-3价,得到电子,作氧化剂,变为还原产物Si3N4。(2)由于反应物的能量比生成物的能量高,多余的能量释放出来。所以该反应是放热反应。(3)①由图像可知M是生成物,N的反应物。在反应方程式中,反应物中只有N2是气体,生成物中只有CO是气体,因此M是CO ,N是N2。②在t2时刻,CO 和N2的物质的量浓度相等,由于反应还没有达到平衡,此时正逆反应速率大小 (正)>
(正)> (逆),反应正向进行。③若t2=2min,从反应开始到t2时刻,V(M)=" (4mol/L-2mol/L)" ÷2min="1mol/(L·min)." ④t3时刻化学反应达到平衡时反应物的转化率为(6mol/L÷8mol/L)×100%="75%" ;(4)①由于A电极失去电子,A极是电池的负极;②Ⅰ. 通入燃料CO的电极为负极,通入氧气的电极为正极。由于b电极通入了氧气,所以该电池的正极为b ;根据同种电荷相互排斥,异种电荷相互吸引的原则,O2-会向正电荷较多的负极移动;Ⅱ.对于该燃料电池来说,正极反应为O2+4e-===2O2- ;负极反应为CO-2e-+O2-===CO2。该电池的总方程式为2CO+O2===CO2。
(逆),反应正向进行。③若t2=2min,从反应开始到t2时刻,V(M)=" (4mol/L-2mol/L)" ÷2min="1mol/(L·min)." ④t3时刻化学反应达到平衡时反应物的转化率为(6mol/L÷8mol/L)×100%="75%" ;(4)①由于A电极失去电子,A极是电池的负极;②Ⅰ. 通入燃料CO的电极为负极,通入氧气的电极为正极。由于b电极通入了氧气,所以该电池的正极为b ;根据同种电荷相互排斥,异种电荷相互吸引的原则,O2-会向正电荷较多的负极移动;Ⅱ.对于该燃料电池来说,正极反应为O2+4e-===2O2- ;负极反应为CO-2e-+O2-===CO2。该电池的总方程式为2CO+O2===CO2。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| | 钾 | 钠 | Na2CO3 | 金刚石 | 石墨 |
| 熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 774 | 882.9 | 1850(分解产生CO2) | --- | 4250 |
 2Na2CO3(1)+C(s,金刚石);△H=-1080.9kJ/mol
2Na2CO3(1)+C(s,金刚石);△H=-1080.9kJ/mol
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题


 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
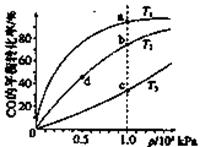
 CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,| 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |
| K | 2.50 | 0.34 | 0.15 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
 2H2↑+O2↑
2H2↑+O2↑ 2H2+O2
2H2+O2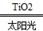 2H2↑+O2↑
2H2↑+O2↑ CO+3H2
CO+3H2 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。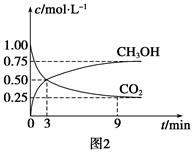
 CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
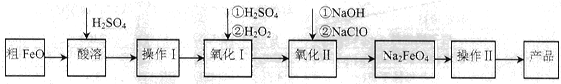
| 温度/℃ | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO浓度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3达到化学平衡状态,下列说法一定正确的是
2NH3达到化学平衡状态,下列说法一定正确的是| A.每1 mol N≡N断裂的同时有2 mol N—H生成 |
| B.N2、H2、NH3的浓度之比为1:3:2 |
| C.N2减少的速率和NH3减少的速率之比为1:2 |
D.气体体积为初始体积的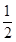 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com