
вбжЊСђЫсЁЂАБЫЎЕФУмЖШгыЫљМгЫЎСПЕФЙиЯЕШчЭМЫљЪОЃЌЯжгаСђЫсгыАБЫЎИївЛЗнЃЌЧыИљОнБэжааХЯЂЃЌЛиД№ЯТСаЮЪЬтЃК

| ШмжЪЕФЮяжЪЕФСП ХЈЖШ/molЁЄL-1 | ШмвКЕФУмЖШ /gЁЄcm-3 |
СђЫс | c1 | Іб1 |
АБЫЎ | c2 | Іб2 |
ЃЈ1ЃЉБэжаСђЫсЕФжЪСПЗжЪ§ЮЊ_____ЃЈВЛаДЕЅЮЛЃЌгУКЌc1ЁЂІб1ЕФДњЪ§ЪНБэЪОЃЉЁЃ
ЃЈ2ЃЉЮяжЪЕФСПХЈЖШЮЊc1 molЁЄL-1ЕФСђЫсгыЫЎЕШЬхЛ§ЛьКЯЃЈЛьКЯКѓШмвКЬхЛ§БфЛЏКіТдВЛМЦЃЉЃЌЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШЮЊ_____molЁЄL-1ЁЃ
ЃЈ3ЃЉЮяжЪЕФСПХЈЖШЮЊc2 molЁЄL-1ЕФАБЫЎгы c2 molЁЄL-1ЕФАБЫЎЕШжЪСПЛьКЯЃЌЫљЕУШмвКЕФУмЖШ_____ ЃЈЬюЁАДѓгкЁБЁЂЁАаЁгкЁБЛђЁАЕШгкЁБЃЌЯТЭЌЃЉІб2 gЁЄcm-3ЃЌЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШ_____
c2 molЁЄL-1ЕФАБЫЎЕШжЪСПЛьКЯЃЌЫљЕУШмвКЕФУмЖШ_____ ЃЈЬюЁАДѓгкЁБЁЂЁАаЁгкЁБЛђЁАЕШгкЁБЃЌЯТЭЌЃЉІб2 gЁЄcm-3ЃЌЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШ_____ c2 molЁЄL-1ЃЈЩшЛьКЯКѓШмвКЕФЬхЛ§БфЛЏКіТдВЛМЦЃЉЁЃ
c2 molЁЄL-1ЃЈЩшЛьКЯКѓШмвКЕФЬхЛ§БфЛЏКіТдВЛМЦЃЉЁЃ
ЃЈ1ЃЉ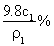 ЃЈ2ЃЉc1/2 ЃЈ3ЃЉДѓгк Дѓгк
ЃЈ2ЃЉc1/2 ЃЈ3ЃЉДѓгк Дѓгк
ЁОНтЮіЁПНтД№БОЬтгІзЂвтвдЯТШ§ЕуЃК
ЃЈ1ЃЉЩшСђЫсЬхЛ§ЮЊ1 LНјааМЦЫуЃЛ
ЃЈ2ЃЉзЂвтМгЫЎЯЁЪЭКѓЃЌПЩШЯЮЊЪЧСНШмвКЕФЬхЛ§КЭЃЛ
ЃЈ3ЃЉгЩЭМЯёПЩжЊЃЌСђЫсЕФУмЖШж№НЅМѕаЁЃЌАБЫЎЕФУмЖШж№НЅдіДѓЁЃ
ЃЈ1ЃЉЩшСђЫсЕФЬхЛ§ЮЊ1 LЃЌдђ

ЃЈ2ЃЉСђЫсгыЫЎЕШЬхЛ§ЛьКЯЃЈКіТдШмвКЬхЛ§ЕФБфЛЏЃЉЃЌШмвКЕФЬхЛ§БфЮЊдРДЕФ2БЖЃЌдђХЈЖШЮЊ molЁЄL-1ЁЃ
molЁЄL-1ЁЃ
ЃЈ3ЃЉИљОнЭМЯёПЩжЊЃЌАБЫЎЕФХЈЖШдНДѓЃЌУмЖШдНаЁЃЌдђc2 molЁЄL-1АБЫЎЕФУмЖШаЁгк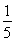 c2 molЁЄL-1АБЫЎЕФУмЖШЃЌЕШжЪСПЪБЃЌ
c2 molЁЄL-1АБЫЎЕФУмЖШЃЌЕШжЪСПЪБЃЌ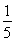 c2 molЁЄL-1АБЫЎЕФЬхЛ§аЁгкc2 molЁЄL-1АБЫЎЕФЬхЛ§ЁЃСНепЛьКЯКѓЃЌЫљЕУШмвКЕФУмЖШвЛЖЈБШІб2ДѓЃЌЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШЧїНќгкЬхЛ§ДѓепЃЌЙЪДѓгк
c2 molЁЄL-1АБЫЎЕФЬхЛ§аЁгкc2 molЁЄL-1АБЫЎЕФЬхЛ§ЁЃСНепЛьКЯКѓЃЌЫљЕУШмвКЕФУмЖШвЛЖЈБШІб2ДѓЃЌЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШЧїНќгкЬхЛ§ДѓепЃЌЙЪДѓгк c2 molЁЄL-1ЁЃ
c2 molЁЄL-1ЁЃ
ЛьКЯШмвКШмжЪжЪСПЗжЪ§ЕФЧѓЫу
ЭЌвЛШмжЪЁЂжЪСПЗжЪ§ЗжБ№ЮЊa%ЁЂb%ЕФСНШмвКЛьКЯЃК
ЃЈ1ЃЉШєСНШмвКЕШжЪСПЛьКЯЃЌдђЛьКЯКѓШмвКжаШмжЪЕФжЪСПЗжЪ§ЕШгк ЃЈa%+b%ЃЉЁЃ
ЃЈa%+b%ЃЉЁЃ
ЃЈ2ЃЉШєЪЧХЈЖШдНДѓЃЌУмЖШдНаЁЕФШмвКЃЌШчАБЫЎЁЂввДМЕШЃЌЕШЬхЛ§ЛьКЯКѓЫљЕУШмвКжаШмжЪЕФжЪСПЗжЪ§аЁгк ЃЈa%+b%ЃЉЁЃ
ЃЈa%+b%ЃЉЁЃ
ЃЈ3ЃЉШєИУШмвКХЈЖШдНДѓЃЌУмЖШдНДѓЃЌШчГЃМћЕФЫсЃЈЯЁСђЫсЃЉЁЂМюЃЈNaOHШмвКЃЉЁЂбЮЃЈNaClШмвКЃЉЕШЃЌЕШЬхЛ§ЛьКЯКѓЫљЕУШмвКжаШмжЪЕФжЪСПЗжЪ§Дѓгк  ЃЈa%+b%ЃЉЁЃ
ЃЈa%+b%ЃЉЁЃ
ЫЕУїЃКЂйШєЪЧгыЫЎЛьКЯЃЌЫЎжаШмжЪЕФжЪСПЗжЪ§ПЩЪгЮЊ0ЁЃ
ЂкСНШмвКЛьКЯЧАКѓЕФжЪСПЪиКуЃЌЬхЛ§ВЛЪиКуЁЃ


 ЕМбЇШЋГЬСЗДДгХбЕСЗЯЕСаД№АИ
ЕМбЇШЋГЬСЗДДгХбЕСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 2-2РызгЗДгІСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЯТСаРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎНЋNaЭЖШыCH3COOHжаЃК2Na+2H+=2Na++H2Ёќ
BЃЎНЋЙ§СПАБЫЎМгШыЕНAlCl3ШмвКжаЃКAl3++4OH-=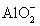 +2H2O
+2H2O
CЃЎЯђТШЛЏвјаќзЧвКжаМгШыфхЛЏМиШмвКЃКAg++Br-=AgBrЁ§
DЃЎЬМЫсЧтИЦШмвКжаМгШыЕШЮяжЪЕФСПЕФЧтбѕЛЏФЦШмвКЃКCa2++ 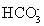 + OH-= CaCO3Ё§+H2O
+ OH-= CaCO3Ё§+H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 11-3ЮяжЪЕФжЦБИСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
гаШчЯТМИжжжЦБИЦјЬхЕФЗНАИЃК
ЂйгУЯЁЯѕЫсгыаПЗлЗДгІжЦЧтЦјЃЛЂкгУЫЎгыЙ§бѕЛЏФЦЙЬЬхЗДгІжЦбѕЦјЃЛЂлГЃЮТЯТгУЬњЦЌКЭХЈСђЫсжЦБИЖўбѕЛЏСђЃЛЂмбѕЛЏИЦгыХЈАБЫЎЗДгІжЦАБЦјЁЃВЛвЫВЩгУЕФЗНАИга( )
A.ЂйЂл B.ЂкЂл C.ЂлЂм D.ЂйЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 11-1ЛЏбЇЪЕбщвЧЦїКЭЛљБОВйзїСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
ИљОнШчЭМУшЪіЃЌЭъГЩЯТСаЮЪЬтЃК

(1)ЙиБеЭМAзАжУжаЕФжЙЫЎМаaЃЌДгГЄОБТЉЖЗЯђЪдЙмжаМгШывЛЖЈСПЕФЫЎЃЌОВжЙКѓШчЭМЃЌХаЖЯAзАжУЪЧЗёТЉЦјЃпЃпЃпЃпЃп(ЬюЁАТЉЦјЁБЁЂЁАВЛТЉЦјЁБЛђЁАЮоЗЈШЗЖЈЁБ)ЃЌРэгЩЪЧЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЁЃ
(2)ЙиБеBзАжУжаЕФжЙЫЎМаaКѓЃЌПЊЦєЛюШћbЃЌЫЎВЛЖЯЭљЯТСїЃЌжСШЋВПСїШыЩеЦПЃЌХаЖЯBзАжУЪЧЗёТЉЦјЃпЃпЃпЃпЃп(ЬюЁАТЉЦјЁБЁЂЁАВЛТЉЦјЁБЛђЁАЮоЗЈШЗЖЈЁБ)ЃЌРэгЩЪЧЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЁЃ
(3)гУМђЕЅЕФЗНЗЈМьбщCзАжУЕФЦјУмадЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЃпЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 11-1ЛЏбЇЪЕбщвЧЦїКЭЛљБОВйзїСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
вЊХфжЦЮяжЪЕФСПХЈЖШдМЮЊ2 molЁЄLЃ1 ЕФNaOHШмвК100 mLЃЌЯТУцЕФВйзїе§ШЗЕФЪЧ( )
AЃЎГЦШЁ7.8 g Na2O2ЙЬЬхЃЌЗХШы250 mLЩеБжаЃЌгУ100 mL СПЭВСПШЁ100 mLеєСѓЫЎЃЌМгШыЩеБжаЃЌЭЌЪБВЛЖЯНСАшжСЙЬЬхШмНт
BЃЎГЦШЁ8 g NaOHЙЬЬхЃЌЗХШы100 mLСПЭВжаЃЌБпНСАшБпТ§Т§МгШыеєСѓЫЎЃЌД§ЙЬЬхЭъШЋШмНтКѓгУеєСѓЫЎЯЁЪЭжС100 mL
CЃЎГЦШЁ8 g NaOHЙЬЬхЃЌЗХШы100 mLШнСПЦПжаЃЌМгШыЪЪСПеєСѓЫЎЃЌеёЕДШнСПЦПЪЙЙЬЬхШмНтЃЌдйМгШыЫЎЕНПЬЖШЃЌИЧКУЦПШћЃЌЗДИДвЁдШ
DЃЎгУ100 mLСПЭВСПШЁ40 mL 5 molЁЄLЃ1NaOHШмвКЃЌЕЙШы250 mLЩеБжаЃЌдйгУСэвЛСПЭВСПШЁ60 mLеєСѓЫЎЃЌВЛЖЯНСАшЯТЃЌТ§Т§ЕЙШыЩеБжа
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 1-2ЮяжЪЕФСПдкЪЕбщжаЕФгІгУСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ФГЕиЫсгъОМьбщГ§КЌH+ЭтЃлcЃЈOH-ЃЉПЩвдКіЪгЃнЛЙгаNa+ЁЂCl-ЁЂ ЁЂ
ЁЂ ЃЌЦфХЈЖШвРДЮЮЊЃКcЃЈNa+ЃЉ=2.3ЁС10-5mol/LЃЌcЃЈCl-ЃЉ=3.5ЁС10-5mol/L,
ЃЌЦфХЈЖШвРДЮЮЊЃКcЃЈNa+ЃЉ=2.3ЁС10-5mol/LЃЌcЃЈCl-ЃЉ=3.5ЁС10-5mol/L,
cЃЈ ЃЉ=2.3ЁС10-5mol/L,cЃЈ
ЃЉ=2.3ЁС10-5mol/L,cЃЈ ЃЉ=1.05ЁС10-5mol/LЁЃдђИУЕиЫсгъЕФpHЮЊЃЈ ЃЉ
ЃЉ=1.05ЁС10-5mol/LЁЃдђИУЕиЫсгъЕФpHЮЊЃЈ ЃЉ
A.3 B.4 C.5 D.6
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 1-2ЮяжЪЕФСПдкЪЕбщжаЕФгІгУСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЯТСаШмвКжаЃЌШмжЪЕФЮяжЪЕФСПХЈЖШЮЊ1 mol/LЕФЪЧЃЈ ЃЉ
AЃЎНЋ40 g NaOHШмгк1 LЫЎЫљЕУЕФШмвК
BЃЎНЋ80 g SO3ШмгкЫЎВЂХфГЩ1 LЕФШмвК
CЃЎНЋ0.5 mol/LЕФNaNO3ШмвК100 mLМгШШеєЗЂЕє50 g ЫЎЕФШмвК
DЃЎКЌKЃЋЮЊ2 molЕФK2SO4ШмвК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАЕЅдЊМьВт ЕкЫФеТЗЧН№ЪєМАЦфЛЏКЯЮяСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
ШчЭМЫљЪОЃЌНЋМзЁЂввСНИізАгаВЛЭЌЮяжЪЕФеыЭВгУЕМЙмСЌНгЦ№РДЃЌНЋввеыЭВФкЕФЮяжЪбЙЕНМзеыЭВФкЃЌНјааЯТБэЫљСаЕФВЛЭЌЪЕбщ(ЦјЬхдкЭЌЮТЭЌбЙЯТВтЖЈ)ЁЃЪдЛиД№ЯТСаЮЪЬтЃК

(1)ЪЕбщ1жаЃЌГСЕэзюжеБфЮЊ_______ЩЋЃЌаДГіГСЕэБфЩЋЕФЛЏбЇЗНГЬЪН_____________________ЁЃ
(2)ЪЕбщ2МзеыЭВФкЕФЯжЯѓЪЧЃКга_______ЩњГЩЃЌМзЭВЛюШћ_______вЦЖЏ(ЬюЁАЯђЭтЁБЁЂЁАЯђФкЁБЛђЁАВЛЁБ)ЁЃЗДгІКѓМзеыЭВФкгаЩйСПЕФВаСєЦјЬхЃЌе§ШЗЕФДІРэЗНЗЈЪЧНЋЦфЭЈШы_______ШмвКжаЁЃ
(3)ЪЕбщ3жаЃЌМзжаЕФ30 mLЦјЬхЪЧNO2КЭN2O4ЕФЛьКЯЦјЬхЃЌФЧУДМзжазюКѓЪЃгрЕФЮоЩЋЦјЬхЪЧ_______ЃЌаДГіNO2гыH2OЗДгІЕФЛЏбЇЗНГЬЪН____________________________ЁЃ
(4)ЪЕбщ4жаЃЌвбжЊЃК3Cl2+2NH3=N2+6HClЁЃМзеыЭВГ§ЛюШћгавЦЖЏЃЌеыЭВФкгаАзбЬВњЩњЭтЃЌЦјЬхЕФбеЩЋБфЛЏЮЊ_______ЁЃзюКѓеыЭВФкЪЃгрЦјЬхЕФЬхЛ§дМЮЊ_______mLЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАЕЅдЊМьВт ЕкСљЁЂЦпеТЛЏбЇЗДгІгыФмСПЫйТЪЦНКтОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
ПЦбЇМввЛжБжТСІгкЁАШЫЙЄЙЬЕЊЁБЕФЗНЗЈбаОПЁЃ
(1)КЯГЩАБЕФдРэЮЊЃКN2(g)+3H2(g) 2NH3(g)ІЄH=-92.4 kJ/molЃЌИУЗДгІЕФФмСПБфЛЏШчЭМЫљЪОЁЃ
2NH3(g)ІЄH=-92.4 kJ/molЃЌИУЗДгІЕФФмСПБфЛЏШчЭМЫљЪОЁЃ

ЂйдкЗДгІЬхЯЕжаМгШыДпЛЏМСЃЌЗДгІЫйТЪдіДѓЃЌE2ЕФБфЛЏЪЧ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
ЂкНЋ0.3 mol N2КЭ0.5 mol H2ГфШыЬхЛ§ВЛБфЕФУмБеШнЦїжаЃЌдквЛЖЈЬѕМўЯТДяЕНЦНКтЃЌВтЕУШнЦїФкЦјЬхбЙЧПБфЮЊдРДЕФ ЃЌДЫЪБH2ЕФзЊЛЏТЪЮЊ ЃЛгћЬсИпИУШнЦїжаH2ЕФзЊЛЏТЪЃЌЯТСаДыЪЉПЩааЕФЪЧ (ЬюбЁЯюзжФИ)ЁЃ
ЃЌДЫЪБH2ЕФзЊЛЏТЪЮЊ ЃЛгћЬсИпИУШнЦїжаH2ЕФзЊЛЏТЪЃЌЯТСаДыЪЉПЩааЕФЪЧ (ЬюбЁЯюзжФИ)ЁЃ
A.ЯђШнЦїжаАДдБШР§дйГфШыдСЯЦј
B.ЯђШнЦїжадйГфШывЛЖЈСПH2
C.ИФБфЗДгІЕФДпЛЏМС
D.вКЛЏЩњГЩЮяЗжРыГіАБ
(2)ИљОнзюаТЁАШЫЙЄЙЬЕЊЁБЕФбаОПБЈЕРЃЌдкГЃЮТЁЂГЃбЙЁЂЙтееЬѕМўЯТЃЌN2дкДпЛЏМС(ВєгаЩйСПFe2O3КЭTiO2)БэУцгыЫЎЗЂЩњЗДгІЃК
2N2(g)+6H2O(l) 4NH3(g)+3O2(g)
4NH3(g)+3O2(g)
ІЄH=+1 530 kJ/mol
гжжЊЃКH2O(l) H2O(g) ІЄH=+44.0 kJ/mol
H2O(g) ІЄH=+44.0 kJ/mol
дђ2N2(g)+6H2O(g) 4NH3(g)+3O2(g) ІЄH= kJ/molЃЌИУЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊK ЃЌПижЦЦфЫћЬѕМўВЛБфЃЌдіДѓбЙЧПЃЌKжЕ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
4NH3(g)+3O2(g) ІЄH= kJ/molЃЌИУЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊK ЃЌПижЦЦфЫћЬѕМўВЛБфЃЌдіДѓбЙЧПЃЌKжЕ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com