
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,
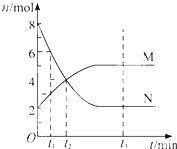
下列表述中正确的是
A.反应的化学方程式为:2 N ![]() M
M
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应在__________min时达到平衡状态;
(2)该反应的化学方程式为_________________________________________________。
(3)反应开始至2 min,气体Z的反应速率为______________________________。
(4)若X、Y、Z均为气体,反应达到平衡时压强是开始时的____________倍;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O。
正极电极反应式为__________________________。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_____,当线路中转移0.4mol电子时,则被腐蚀铜的质量为_______g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)如图是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,A极为电源______(填“正”或“负”)极,写出A极的电极反应式:____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有在室温的条件下,pH均为a的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+)·c(OH)=________________。
(2)各取5 mL上述溶液,分别加水稀释至50 mL,pH较大的是___________溶液。
(3)各取5 mL上述溶液,分别加热到90℃,pH较小的是___________溶液。
(4)H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)分别为_________、__________。
(5)取5 mL NH4Cl溶液,加水稀释至50 mL,c(H+)_________10(a+1)mol·L1(填“>”“<”或“=”),![]() ___________(填“增大”“减小”或“不变”)。
___________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作错误的是( )
A. 滴定管经蒸馏水洗净后,即可注入标准液进行滴定
B. 玻璃导管蘸水后,边旋转边向橡皮管中插入
C. 滴定用锥形瓶经蒸馏水洗净后,不须用标准液润洗
D. 用玻璃棒蘸取待测液滴到pH试纸上,然后跟标准比色卡相对照,读出pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1 mol/L的NaOH溶液滴定20 mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是

A.X=20
B.HA溶液加水稀释后,溶液中![]() 的值减小
的值减小
C.0.1 mol/L的NaOH溶液中,由水电离出的c(OH)=0.1 mol/L
D.加入NaOH溶液体积为X mL时,溶液中c(A)=0.05 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生活动小组设计如图所示装置探究工业制硫酸接触室的反应,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。

试填空:
(1)装置B有三个作用:除了通过观察气泡控制氧气和二氧化硫的速率和比例外,还可以_______和_____。
(2)实验过程中,当V2O5表面红热后,应将酒精灯移开一会儿后再继续加热,其原因是___________。
(3)D中锥形瓶中盛放的溶液可以是(选填序号)____
a、澄清石灰水 b、小苏打溶液 c、氯化钡溶液 d、硝酸钡溶液
反应停止后,要根据装置D锥形瓶中产生的白色沉淀的量,测定已被氧化的二氧化硫的量时,在滤出沉淀前必须进行的一步操作是____________________。
(4)若从锥形瓶溶液中得到的沉淀质量为mg,要测定该条件下SO2的转化率,实验时还需要测定的数据是(选填序号)______。SO2的转化率是_______(用含有m、a、b、c、d中的一种或几种字母的代数式表示)。
①装置F增加的质量ag ②装置A中亚硫酸钠减少的质量bg
③装置B增加的质量cg ④装置E增加的质量dg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 碳酸氢铵溶液与少量氢氧化钠溶液:NH![]() +HCO
+HCO![]() +2OH-===NH3·H2O+CO
+2OH-===NH3·H2O+CO![]() +H2O
+H2O
B. 氯化铵溶液中加入少量稀氢氧化钠溶液:NH![]() +OH-===NH3↑+H2O
+OH-===NH3↑+H2O
C. 氨水与盐酸反应:NH3·H2O+H+===NH![]() +H2O
+H2O
D. 氨水中通入过量二氧化碳:2NH3·H2O+CO2===2NH![]() +CO
+CO![]() +H2O
+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com