
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
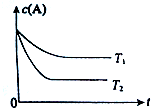 反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如右图所示.回答下列问题:
反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如右图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、缺铁会引起贫血 |
| B、缺钙易患佝偻病或发生骨质疏松 |
| C、缺碘易患坏血病 |
| D、缺锌会引起生长迟缓、发育不良 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用排饱和食盐水法收集Cl2 |
| B、棕红色NO2加压后颜色先变深后变浅 |
| C、打开汽水瓶时,有大量气泡溢出 |
| D、H2、I2、HI平衡混和气加压后颜色变深 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com