
| A.处理过程中银器一直保持恒重 |
| B.银器为正极,Ag2S被还原生成单质银 |
| C.该过程中总反应为2Al + 3Ag2S =" 6Ag" + Al2S3 |
| D.黑色褪去的原因是黑色Ag2S转化为白色AgCl |
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:不详 题型:单选题
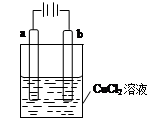
| A.若a和b为石墨,通电后a电极上发生的反应为2Cl--2e-=Cl2↑ |
| B.若a和b为石墨,通电后b电极上发生氧化反应 |
| C.若a为铜,b为铁,通电后a电极质量增加 |
| D.若a为铜,b为铁,通电后Cu2+向铁电极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
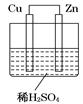
| 实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③ 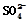 向Cu极移动 向Cu极移动④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu―→Zn ⑥正极反应式:Cu—2e-===Cu2+,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电池内部电子从正极流向负极 |
| B.负极电极反应式为:CH4-8e- + 10OH-=CO32-+ 7H2O |
| C.正极电极反应式为:O2 + 4e-=2O2- |
| D.每消耗22.4 L CH4,外线路中将通过8 mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电池的正极反应式为:O2十2H2O十4e-=4OH- |
| B.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 |
| C.电解后c(Na2CO3)变小 |
| D.电池中c(KOH)不变;电解池中溶液pH变大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
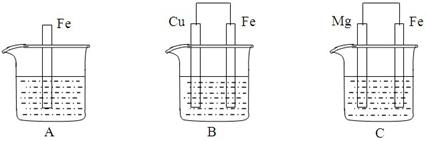
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
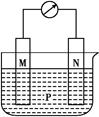
| 选项 | M | N | P |
| A | 锌 | 铜 | 硫酸铜溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.锌是正极,MnO2是负极 | B.锌是负极,MnO2是正极 |
| C.锌是正极,石墨棒是负极 | D.锌是负极,石墨棒是正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com