
 在50mL过氧化氢溶液中加入0.1mol MnO2粉末,标准状况下放出气体的体积和时间的关系如图所示.
在50mL过氧化氢溶液中加入0.1mol MnO2粉末,标准状况下放出气体的体积和时间的关系如图所示.分析 (1)反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应为不可逆反应,在4min后,收集到的气体体积不再增加,说明过氧化氢完全分解,根据图象可知生成的氧气的体积;
(2)反应放出气体体积为气体总体积一半为30mL,根据图象判断需要的时间;
(3)根据浓度对反应速率的影响判断A、B、C、D各点反应速率大小;
(4)0~2min时O2的平均反应速率等于$\frac{V}{t}$.
解答 解:(1)由反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应为不可逆反应,在4min后,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可知,生成氧气的体积为60mL,
故答案为:60mL;
(2)由图象可知,当时间进行到1min时,生成氧气的体积为30mL,此时生成的氧气为总体积的一半,需要的时间为1min,
故答案为:1min;
(3)反应物浓度大小决定反应速率大小,随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小,
故答案为:D>C>B>A;随反应进行c(H2O2)减小,反应物浓度减小,减慢反应速率;
(4)0~2min时O2的平均反应速率等于$\frac{V}{t}$=$\frac{45ml}{2min}$=22.5mL•min-1,故答案为:22.5.
点评 本题考查过氧化氢分解的速率曲线,题目难度不大,主要考查浓度对反应速率的影响,正确分析图象的曲线变化是解答本题的关键.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子间所发生的碰撞为有效碰撞 | |
| B. | 由C(s,石墨)=C(s,金刚石)△H>0可知,金刚石比石墨稳定 | |
| C. | NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| D. | 有气体参与的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子总数,从而使反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是甲烷与乙烷的混合物 | B. | 可能是甲烷与丙烷的混合物 | ||
| C. | 一定含有乙烷 | D. | 可能是甲烷与己烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L水含有NA个水分子 | |
| B. | 氧气和臭氧的混合物32 g中含有NA个氧原子 | |
| C. | 0.1mol Na2O2与水反应时转移0.1NA个电子 | |
| D. | 11.2 L氯气中含有NA个氯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3°C | 78.5°C | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气既能用浓硫酸干燥也能用无水CaCl2干燥 | |
| B. | NH3是电解质,所以氨水能导电 | |
| C. | 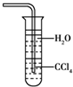 用水吸收NH3用如图装置可防止倒吸 | |
| D. | NH3可以使干燥的红色石蕊试纸变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol•L-1的NaCl溶液中取出10mL,其浓度仍为1mol•L-1 | |
| B. | 配制0.5L1mol•L-1的盐酸,需要氯化氢气体11.2L(标准状况) | |
| C. | 将40gNaOH溶于1L水中,所得溶液的物质的量浓度为1mol/L | |
| D. | 0.5L2mol•L-1BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改进汽车尾气净化技术,减少大气污染物的排放 | |
| B. | 开发利用可再生能源,减少化石燃料的使用 | |
| C. | 研发可降解高分子材料,减少“白色污染冶 | |
| D. | 过度开采矿物资源,促进地方经济发展 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com