
科目:高中化学 来源: 题型:
使用酸碱中和滴定的方法,用0.01mol/L盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作能够使测定结果偏高的是:
A.用量筒量取浓盐酸配制0.01mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸
B.配制稀盐酸定容时,俯视容量瓶刻度线
C.滴定前尖嘴处无气泡,滴定终点时有气泡
D.滴定过程中用少量蒸馏水将锥形瓶内避粘附的盐酸冲下
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(1),氨水]吸收在生产过程中产生的CO和CO2等气体,铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac(Ac表示醋酸根)
[Cu(NH3)3CO]Ac(Ac表示醋酸根)
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是 。(选填编号)
a. 减压 b. 增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)。
.
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
通过比较 可判断氮、磷两种元素的非金属性强弱。
(5)已知CS2和CO2分子结构相似,CS2的电子式是
CS2熔点高于CO2,其原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中对应关系正确的是( )
| A | CH3CH3+Cl2 CH2===CH2+HCl―→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br-===2Cl-+Br2 Zn+Cu2+===Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O===4NaOH+O2↑ Cl2+H2O===HCl+HClO | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有
A、15种 B、28种 C、32种 D、40种
| 酯 | 酸的数目 | 醇的数目 |
| H-COO-C4H9 | 1种 | 4种 |
| CH3-COO-C3H7 | 1种 | 2种 |
| C2H5-COO-C2H5 | 1种 | 1种 |
| C3H7-COO-CH3 | 2种 | 1种 |
| 共计 | 5种 | 8种 |
从上表可知,酸一共5种,醇一共8种,因此可组成形成的酯共计:5×8=40种。
查看答案和解析>>
科目:高中化学 来源: 题型:
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
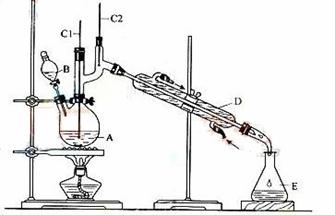
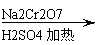 发生的反应如下:
发生的反应如下:
CH3CH2CH2CH2OH CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/ | 密度/(g·cm-3) | 水中溶解性 | |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将 Na2Cr2O7溶液加到浓硫酸中,说明理由
。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法是 。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”
(6)反应温度应保持在90—95℃,其原因是 。
(7)本实验中,正丁醛的产率为 %。
查看答案和解析>>
科目:高中化学 来源: 题型:
华法林是一种治疗心脑血管疾病的药物,可由化合物E和M在一定条件下合成得到(部分反应条件略)
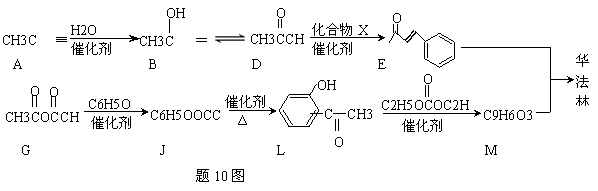

⑴A的名称为 ,A B的反应类型为
B的反应类型为
⑵D E的反应中,加入的化合物X与新制Cu(OH)2反应产生砖红色沉淀的化学方程式为
E的反应中,加入的化合物X与新制Cu(OH)2反应产生砖红色沉淀的化学方程式为
⑶G J为取代反应,其另一产物分子中的官能团是
J为取代反应,其另一产物分子中的官能团是
⑷L的同分异构体Q是芳香酸,Q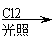
 R(C8H7O2Cl)
R(C8H7O2Cl)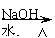
 S
S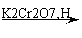
 T,T的核磁共振氢谱只有两组峰,Q的结构简式为
T,T的核磁共振氢谱只有两组峰,Q的结构简式为  ,R
,R S的化学方程式为
S的化学方程式为
⑸题 10图中,能缩合成体型高分子化合物的酚类单体是
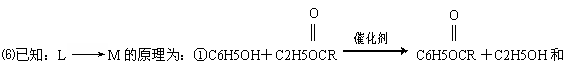

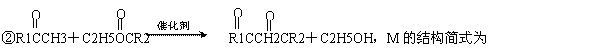

查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂方案正确的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | CO2(g) | SO2(g) | 饱和NaHSO4溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C | Cl2(g) | HCl(g) | 饱和NaHCO3溶液、浓H2SO4 | 洗气 |
| D | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空
(1)写出B、D的化学式:B ,D 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(3)在A溶液中加少入量澄清石灰水,其离子方程式为 。
(4)C常用作净水剂,用离子方程式表示其净水原理 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com