
【题目】液氨-液氧燃料电池曾用于驱动潜艇,其示意图如图所示,下列有关说法不正确的是

A. 电极2是正极,发生还原反应
B. 电池工作时,Na+向电极1移 动
C. 电流由电极2经外电路流向电极1
D. 电极1发生的电极反应为:2NH3+6OH--6e-= N2↑ +6H2O
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】(1)下列四种物质,①NA个HCl ②24gCH4 ③4.816×1023个H2O2分子 ④10.8mL水(密度为1g·cm-3)。
ⅰ.四种物质所含分子数由多到少的顺序是:_________________________________;
ⅱ.四种物质所含原子数由多到少的顺序是:_________________________________;
ⅲ.四种物质所含H由多到少的顺序是:_____________________________________;
ⅳ.四种物质的质量由多到少的顺序是:_____________________________________。
(2)H2O与CO2的质量比为18:22,则H2O和CO2的物质的量之比为________,分子个数比为_______,原子个数比为__________,所含氧原子个数比为___________。
(3)在标准状况下,等质量的O3和CO2比较,密度比为________,分子数之比为_________,原子数之比______,体积比为_______,物质的量之比__________。
(4)CH4与H2的混合气体,其质量百分含量分别为80%、20%,则混合气体的平均相对分子质量为__________。
(5)标准状况下,某气体密度为1.96g/L,则该气体的摩尔质量为_____(保留整数)
(6)把100克某NaOH溶液(密度是1.22g/cm3)蒸发浓缩,余下溶液50ml时,物质的量浓度是8mol/L,原溶液的物质的量浓度是 _________________。
(7)已知Na2S、Na2SO3、Na2SO4混合物中硫元素的质量分数为a%,则氧元素的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在标准状况下的四种气体①6.72LCH4②3.01×1023个HCl分子③13.6gH2S④0.2molNH3,密度最大的是_____(填序号)。
(2)标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为7.6g,则混合气体中甲烷的体积分数为_______。
(3)某物质A加热时按化学方程式2A═2B+C+3D分解,产物均为气体,测得由生成物组成的混合物气体对H2的相对密度为20,则反应物A的摩尔质量为____________。
(4)80 g密度为1 gcm-3的CaCl2溶液里含2 g Ca2+,从中再取出一半的溶液中Cl-的物质的量浓度是_______。
(5)10 mL 0.1 mol·L-1 BaCl2溶液恰好使相同体积的硫酸铁、硫酸铜两种溶液中的SO42-完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiO2是一种性能优良的半导体光催化剂,能有效地吸附有机污染物(如甲醛、甲苯等)和含氮化合物(如NH3、CN-等)转化为CO2和N2等小分子物质。
(1)Ti基态核外电子排布式为________________。
(2)甲醛HCHO分子空间构型为_____;分子中碳原子轨道杂化类型为_____,π键和σ键的个数之比为____,
(3)氨气极易溶于水,是因为氨和水的分子均是_________,还因为___________。
(4)甲苯分子中能够共平面的原子最多为____个;苯环不易被卤素加成,而比较容易被卤素取代苯环上的氢,原因是___________________。
(5)含CN-的污水毒性极大,用NaClO先把CN-氧化为CNO-,然后在酸性条件下再将CNO-氧化为无污染的气体。请写出与CNO-互为等电子体的微粒______分子或离子,写一种)。
(6)Ti[(CN)4]2-中Ti2+与CN-的C原子形成配位键。不考虑空间构型,Ti[(CN)4]2-的结构可表示为_____________________。
(7)Ti的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+位于立方体的顶点,Ca2+ 处于立方体的中心)。该晶体中,Ti4+和周围____ 个O2-相紧邻;若该晶胞的密度为dg/cm3则钛氧键的键长为______pm (用带NA的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 不同类型的洗涤剂混合使用能够增加其洗涤效果
B. 不同的消毒剂混合使用能够增加其消毒功能
C. 天然的洗涤剂的去污效果比合成的好
D. 增白洗涤剂中的增白剂本身没有去污能力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子可以在溶液中大量共存的是( )
A.K+、Mg2+、SO42﹣、OH﹣
B.Na+、H+、Cl﹣、HCO3﹣
C.K+、Ag+、NO3﹣、Cl﹣
D.K+、Cu2+、SO42﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂的存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应由苯A制备化合物E的一种合成路线:


回答下列问题:
(1)B的结构简式为________,D的化学名称为________。
(2)①和③的反应类型分别为________、________。
(3)E的结构简式为____________________。1 mol E与氢气反应,理论上最多消耗氢气________ mol。
(4)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3∶1,则符合条件的同分异构体有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)立方烷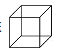 它的六氯代物有____种。
它的六氯代物有____种。
(2)  分子中最多有个____原子共面.
分子中最多有个____原子共面.
(3)① ![]() 的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
②聚合物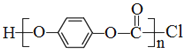 的单体是__________________。
的单体是__________________。
(4)①写出![]() 与足量溴水反应的化学方程式__________。
与足量溴水反应的化学方程式__________。
②写出 与足量NaOH溶液反应的化学方程式________。
与足量NaOH溶液反应的化学方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com